日外会誌. 124(6): 500-506, 2023
特集
先天性嚢胞性肺疾患のup to date
6.外科治療2.小児に対する胸腔鏡手術の現況
|
名古屋大学大学院 小児外科学 内田 広夫 |
2000年に先天性嚢胞性肺疾患に対する胸腔鏡下肺葉切除術が小児ではじめて報告されてから急速に普及し,現在日本でも約200例(60%)で胸腔鏡下肺切除が行われている.先天性嚢胞性肺疾患の80%は胎児診断され,そのなかの15%が出生後早期に呼吸困難等の症状を起こす.症状がある新生児に対しては早期手術が行われ,以前では開胸手術が行われていたが,現在では胸腔鏡でも安全に施行可能であることがわかってきた.無症状の患児に対して,手術を行うべきか,いつ手術を行うべきかに関しては,まだ確定していない部分もあるが,ほとんどの患児で嚢胞の感染が起きることから,当科では生後6カ月以内に手術を行っている.多くのメタアナリシスによって,胸腔鏡手術は開胸と比較して,術中,術後の合併症は増加せず,ドレーン抜去や入院期間が短くなることが示されている.肺炎などの急性炎症が収まった後に胸腔鏡手術は行うべきであること,術者の熟達度があがることで開胸移行が減少することが言われているが,患者年齢,嚢胞の大きさなどは開胸移行とは関係ないことが示されてきた.内視鏡手術機器の進歩もあり,胸腔鏡手術を行うチームおよび術者に十分な知識と技量があれば,新生児,乳児でも安全に胸腔鏡手術は施行可能である.
キーワード
胸腔鏡下肺切除, 開胸, 小児, 胎児診断, 先天性嚢胞性肺疾患
I.はじめに
2000年に肺嚢胞性疾患に対する胸腔鏡下肺葉切除術が小児ではじめて報告され1),2003年には胸腔鏡下肺葉切除術が開胸手術と比較して,周術期の合併症が増加することなく,入院期間が短く,胸腔ドレーン挿入期間が短いことがはじめて示された2).その後胸腔鏡下肺切除術は急速に普及し,日本の小児外科施設でも肺切除の胸腔鏡手術は2013年には327例中135例(41.3%)であったが,2019年には316例中193例(61.1%)と増加している.この項では,先天性嚢胞性肺疾患に対する胸腔鏡下肺切除の適応や時期,安全性,意義について述べたい.
II.先天性嚢胞性肺疾患に対する手術適応
胎児期に先天性嚢胞性肺疾患(CCLD)と診断される患児は増加しており,CCLDの重症度は胎児エコーを用いてvolume to head circumference (CVR)などを測定することで継続的に評価される.胎児水腫を呈する患児は多くはないが,そのような重症な場合は母体へのステロイド投与,胸腔羊水腔シャントなどの治療が行われる.一方で肺炎や気胸でみつかるCCLDはおよそ5分の1程度と言われている.CCLDと診断され,出生した患児のおおよそ15%程度で呼吸障害を認めることが知られている.新生児期に呼吸状態が安定しない場合は早期手術が必要となり,そのような呼吸障害がある場合,開胸手術が選択されることが多かったが,最近では胸腔鏡でも合併症は増加せず安全に行えることが示されている3).出生時に症状がない患者に対しては,手術をするべきか,手術を行う時期はいつがよいかに関してはいまだにcontroversyである.手術をするべきかどうかに関しては,ほとんどの症例がいずれ感染を起こす可能性が非常に高いことから,手術が必要と言われている4)がこれらの観察は手術を原則としている小児外科施設で行われており,今後手術の適応に関して,変更となる可能性は否定できない.1歳以内で肺に感染を引き起こす確率は10~30%と言われており5),肺嚢胞の感染が起きると,術中,術後合併症が高率に起きること,術後入院期間が延長することが報告されている6).また生後早期に手術をすることで残った肺機能の改善が良いことも示されている7)が,長期間の前方視的観察研究では,肺機能の改善と手術時期には関わりがなかったという報告8)もある.このように手術時期に関してはまだ完全には定まっていないが,われわれはこれらの報告を参考にして,出生時期に呼吸症状のないCCLDに対しては,生後6カ月以内に胸腔鏡手術を行う方針としている9).
III.胸腔鏡手術の適応
手術の必要性,手術時期が決まった時点で,胸腔鏡で行うべきか,開胸で行うべきかを決めなければならない.新生児期で呼吸循環状態が非常に不安定な場合は,開胸手術が選択されることが多い.呼吸循環状態が落ち着いているようなCCLDに対して,開胸手術と胸腔鏡手術を比較したメタアナリシスでは,両者の手術合併症は変わらないが,胸腔鏡手術のほうが胸腔ドレーンを抜去するまでの時間や入院期間が短いとする報告も多い10)
~
12).開胸へ移行した症例を検討すると,術前の呼吸器症状があると肺炎などの感染が高率に認められるため,少なくとも急性炎症が改善した時点で胸腔鏡は行うべきである.最近の報告では呼吸器感染症状が改善したあとで胸腔鏡手術を行うと,合併症は開胸と変わりがないことが報告されている13).開胸への移行は術者の経験と関わっているという報告もあるが,患者の年齢や病変の大きさは術後合併症や開胸移行率と関係ないと言う報告が多い14)15).
IV.術前評価
多くのCCLDは胎児診断されているため,呼吸器症状があるかないかによって手術のタイミングや方法は変わってくる.CVRが0.84より大きい場合は出生時に呼吸器症状が増加すると言われている16).呼吸困難が強い場合は,それに応じた治療を行い,改善がみられた時点で,開胸手術が選択されることが多いが胸腔鏡手術も可能である.呼吸器症状が落ち着けば造影CTを行って解剖学的評価を行ったのち手術を行う.
V.手術時麻酔および体位
麻酔導入時,片肺換気のために気管支ブロックなどが行われるが,1歳以下の乳児では片肺換気は難しい.年長児であれば成人と同様にダブルルーメンによる片肺換気が行われる.当科では乳児などは片肺換気を行っておらず,陽圧気胸によって術野を確保して手術を行っている.気管支ブロッカーによる片肺換気は12kg以上,ダブルルーメンによる片肺換気は30kg以上を目安としている.麻酔導入後,病変部を上とした側臥位をとる.体位がずれないように,また体重による圧が分散するようにパットを引きつめ患児を固定する.
VI.手術手技
体位およびポート挿入
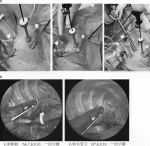
術者,スコピストは手術台の同じ側,助手はその反対側に立つ.術者の立ち位置は出血した場合に最も危険な肺静脈の処理を体格の小さな患児でも安全に行えるように,処理する肺静脈の位置の対側としている.つまり上,中葉切除を行う場合は肺静脈の処理は腹側であるため,背側に立ち,下葉切除を行う際は,肺静脈の処理は背側であるため,腹側に立つ(図1a,b).First portは第6肋間にOptical Trocarを用いて肺を観察しながら挿入する.ポート挿入後,気胸圧6mmHg,送気流量1L/minとして肺がある程度押しつぶされるのを確認しながら5mm 30度斜視スコープを挿入する.前後の肋間に術者操作用の5mmポートをそれぞれ挿入し,助手ポートとして3mmポートをひし形を作るように配置する.助手のポートで肺の牽引を行い,カウンタートラクションをかけながら手術操作を行う.
肺動静脈・気管の処理
肺の癒着などを切除し,肺をフリーの状態とする.上葉切除の場合は肺門部の処理から開始する.基本的には肺動脈を処理後,肺静脈の処理を行うが,右上葉のように肺静脈の処理を行わないとA2の処理が難しいような場合は,肺静脈を先に処理する.葉間を確認し,分葉不全がある場合は電気メスを用いて葉間を作成する.分葉不全が強い場合は,vessel sealing systemなどを用いて葉間を作成することもあるが,できるかぎり電気メスで葉間を明らかにしている.葉間が確認できれば,切除する肺葉に向かう動脈を順番に切離していく.肺静脈には大きなvariantsは少なく肺門部での処理は定型的に行うことが可能である.肺動脈と肺静脈を処理すると切除するべき肺葉へ向かう気管が明らかになるので,ダブルクリップもしくは自動縫合器を用いて切離を行う.12mmの自動縫合器は体格の小さい乳児では挿入後自由に取り回しが難しいため,5mm自動縫合器を使用することもあるが,気管の剛性によってはこの自動縫合器では気管支瘻となる可能性があるため,アンビル幅6.3mm,シャフト径8mmの自動縫合器を使用することが多い.これを使用する際は5mmポートを抜去し,直接胸腔内に挿入して使用している(図2a,b).
切除肺の摘出と胸腔ドレーンの挿入
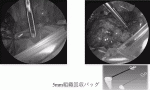
切除肺は,5mm組織回収バッグを使用する.通常の5mm組織回収バッグは組織挿入口を広げることが難しいが,ワイヤーが通してあるTKバッグは内筒を押し込むことで口が開くため,その他の5mmの組織回収バッグと比較して摘出組織の格納が格段に行いやすい(図3).バッグ内に摘出肺を収め,ポート創部を延長せず,肺をバッグ内で細断して摘出する.ドレーンは12もしくは14Frのドレナージチューブを留置する.
胸腔鏡下肺区域切除術
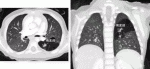
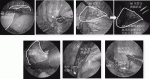
CCLDに対する胸腔鏡下肺葉切除術が標準術式として確立された今,CCLDを過不足なく切除する肺区域切除が試みられている.解剖学的な区域切除が必要であるため,正確な区域レベルでの肺動静脈,気管支の理解が必要となる.先天性肺気道奇形では病変は肺区域内にとどまらずに広がり,気管支閉鎖では閉鎖した領域の肺は過膨脹するため,大きく広がっている.これらから,正確な区域切除を行うことは非常に難しい9).しかし,明らかに小さな区域内にとどまるような病変に対しては肺葉切除ではなく肺区域切除が望ましい.今後は正常な組織をできる限り残すという,本当の意味での低侵襲手術へと向かう必要がある.当科でも積極的に区域切除を行っており,1歳5カ月,8.7kg,左S6の気管支閉鎖症に対して,S6区域切除を行った症例を提示する(図4).A6の切離後,ICGで血流が遮断された領域とCT,肉眼での病変から,切離範囲を決定し,V6を切離後,自動縫合器でS6区域切除を終えた(図5).詳細は前のテーマを参照していただきたい.
合併症と術後管理
術中,術後合併症は開胸と変わらないことが示されている.術中出血は最も危険な合併症であり,開胸移行の主たる原因となっている.術後継続する気瘻,気胸は10% 以下,術後肺炎は5~10%と報告されている.術後管理は開胸手術と同じで,術後すぐに経口を開始でき,気胸がなければ胸腔ドレーン抜去をし,すぐに退院することが可能である.
長期予後
長期予後は良好である.呼吸機能に関しては,術後ほぼ正常となることが示されている.また,長期的には開胸と比較して,呼吸機能がより改善しているという報告もある17).

VII.おわりに
先天性嚢胞性肺疾患は多くの場合胎児診断される.大きな病変の場合は,胎児の血行動態や出生後の呼吸障害を引き起こすが,多くの患児では明らかな症状を示さない.悪性が疑われる場合や感染が起きることが予想される場合は,早期に切除する必要があるが,通常無症状のため待機的に手術が行われる.胸腔鏡下肺切除術は開胸手術と比較して,術中,術後合併症のリスクは同程度で,ドレーン挿入期間や入院期間を短縮し,さらに術後の長期観察でも胸郭変形が少なく,肺機能が同等もしくは良好であることが示されている.これらから患児の状態が胸腔鏡手術に耐えられると考えられる場合には積極的に選択されうる.外科医の技術および内視鏡手術機器の進歩により,新生児,乳児でも安全に胸腔鏡手術が可能である.
利益相反:なし
文献
1) Rothenberg SS: Thoracoscopic lung resection in children. J Pediatr Surg, 35: 271-274 ; discussion 274-275, 2000.
2) Albanese CT, Sydorak RM, Tsao K, et al.: Thoracoscopic lobectomy for prenatally diagnosed lung lesions. J Pediatr Surg, 38: 553-555, 2003.
3) Zheng J, Tang H, Xu H, et al.: Thoracoscopic versus open resection for symptomatic congenital pulmonary airway malformations in neonates:a decade-long retrospective study. BMC Pulm Med, 21: 82, 2021.
4) Kuroda T, Nishijima E, Maeda K, et al.: Clinical Features of Congenital Cystic Lung Diseases:A Report on a Nationwide Multicenter Study in Japan. Eur J Pediatr Surg, 26: 91-95, 2016.
5) Stanton M, Njere I, Ade-Ajayi N, et al.: Systematic review and meta-analysis of the postnatal management of congenital cystic lung lesions. J Pediatr Surg, 44: 1027-1033, 2009.
6) Aspirot A, Puligandla PS, Bouchard S, et al.: A contemporary evaluation of surgical outcome in neonates and infants undergoing lung resection. J Pediatr Surg, 43: 508-512, 2008.
7) Beres A, Aspirot A, Paris C, et al.: A contemporary evaluation of pulmonary function in children undergoing lung resection in infancy. J Pediatr Surg, 46: 829-832, 2011.
8) Naito Y, Beres A, Lapidus-Krol E, et al.: Does earlier lobectomy result in better long-term pulmonary function in children with congenital lung anomalies? A prospective study. J Pediatr Surg, 47: 852-856, 2012.
9) Shirota C, Tainaka T, Sumida W, et al.: Thoracoscopic surgery for congenital lung cysts:an attempt to limit pulmonary resection in cases of lesions involving multiple lobes. Pediatr Surg Int, 37: 213-221, 2021.
10) Nasr A, Bass J: Thoracoscopic vs open resection of congenital lung lesions:a meta-analysis. J Pediatr Surg, 47: 857-861, 2012.
11) Rahman N, Lakhoo K: Comparison between open and thoracoscopic resection of congenital lung lesions. J Pediatr Surg, 44: 333-336, 2009.
12) Vu LT, Farmer DL, Nobuhara KK, et al.: Thoracoscopic versus open resection for congenital cystic adenomatoid malformations of the lung. J Pediatr Surg, 43: 35-39, 2008.
13) Seong YW, Kang CH, Kim JT, et al.: Video-assisted thoracoscopic lobectomy in children:safety, efficacy, and risk factors for conversion to thoracotomy. Ann Thorac Surg, 95: 1236-1242, 2013.
14) Boubnova J, Peycelon M, Garbi O, et al.: Thoracoscopy in the management of congenital lung diseases in infancy. Surg Endosc, 25: 593-596, 2011.
15) Garrett-Cox R, MacKinlay G, Munro F, et al.: Early experience of pediatric thoracoscopic lobectomy in the UK. J Laparoendosc Adv Surg Tech A, 18: 457-459, 2008.
16) Ruchonnet-Metrailler I, Leroy-Terquem E, Stirnemann J, et al.: Neonatal outcomes of prenatally diagnosed congenital pulmonary malformations. Pediatrics, 133:e1285-1291, 2014.
17) Lau CT, Wong KKY: Long-term pulmonary function after lobectomy for congenital pulmonary airway malformation:is thoracoscopic approach really better than open? J Pediatr Surg, 53: 2383-2385, 2018.
PDFを閲覧するためには Adobe Reader が必要です。