日外会誌. 125(2): 131-138, 2024
特集
外科におけるRCT―top journalへの道―
6.下部消化管外科におけるRCT―top journalへの道―
|
大分大学 消化器・小児外科 赤木 智徳 , 猪股 雅史 |
本邦発信の下部消化管外科手術療法に関する大規模なRandomized clinical trial(RCT)は,約20年前にJCOG(日本臨床腫瘍研究グループ)大腸がんグループで計画立案されたJCOG0404試験,そしてJCOG0212試験,JOCG1006試験が最初である.手術療法のRCTとして,全国の多くの施設,大腸外科医が参加し,試験計画立案時から多くの時間をかけ詳細なプロトコールを作成し,症例登録,結果解析をすすめてきた試験である.試験遂行のためには多くの課題を克服し,クリニカルクエスチョンを解決し,その結果トップジャーナルに掲載されている.今回,3試験の概要,試験遂行のための取り組み,今後の展望を述べる.現在,これらの試験結果からさらなるクリニカルクエスチョンが創出され,後継試験がすすんでいる.進行中の試験は,手術療法に化学放射線療法が加わり多岐のモダリティを駆使した集学的治療の新規治療開発を目指しており,その結果が期待される.
キーワード
大腸外科, RCT 手術療法, クオリティコントロール・クオリティアシュアランス
I.はじめに
外科手術治療に関するRCTでは,臨床試験に参加する施設や外科医の数が複数必要である.そのため,手術手技にかかわるクオリティコントロール・クオリティアシュアランスがとても重要となる.この点が医薬品の臨床試験と大きく異なる点の一つと考えられる.従って,臨床試験のプロトコールを作成する際には,手術手技とくに試験治療の手術手技のバラツキを最小限に抑えるためにプロトコールに手術手技の詳細を記載する必要がある.JCOG0404,JCOG0212,JCOG1006試験は,手術手技の詳細をプロトコールに記載することに加えて,手術手技の核となる,リンパ節郭清完了後の術中写真提出を全登録症例に求められている.それをもとに画像中央判定を行い,手技の確認・統一化を図り臨床試験の手術手技のクオリティを高く設定することが可能となっている.本邦において下部消化管外科手術手技に関する臨床試験を行い,トップジャーナルに掲載された上記3試験について,また今後の下部消化管外科手術手技に関する臨床試験の展望について述べる.
II.JCOG0404試験(腹腔鏡手術は開腹手術と比べ有用か)
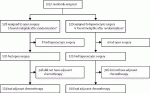
JCOG0404試験では,cStage Ⅱ/Ⅲの結腸癌患者を対象に,腹腔鏡下手術(LAP)の開腹手術(OP)に対する有用性の検証を非劣性デザインにて計画された(図1).その結果,主要評価項目である全生存期間においてLAPのOPに対する非劣性は統計的に証明されなかったが,試験計画時の想定を上回る良好な生存曲線から,サブグループ解析により臨床的にLAPが劣っているかもしれないと懸念される対象(high BMI,T4,N2)に注意すれば,標準治療のオプションとして許容されると結論づけられた(図2)(Kitano S. Lancet Gastroenterol Hepatol 2: 261-268, 2017)1).
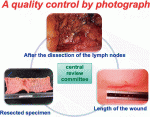
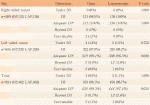
本試験はJCOG大腸がんグループで計画された初めての手術療法に関する第3相試験であった.試験遂行における克服すべき重要な問題点は,手術手技のクオリティコントロール・クオリティアシュアランスの確保の困難性,試験参加同意取得の困難性があった.手術手技のバラツキをなくすために,手術手技の詳細,術者基準を設定し,さらに全登録症例に対して手術手技の核となる術中写真3枚の提出(図3)をプロトコールに記載されている.それをもとに画像中央判定を行い,手技の確認・統一化を図っている.その結果,本試験の手術手技のクオリティコントロール・クオリティアシュアランスが十分に確保できたことがサブ解析にて判明している(Nakajima K. Jpn J Clin Oncol. 2014 Sep; 44(9): 799-806.)2).その結果は,右側左側結腸癌において開腹手術では99.3%,腹腔鏡手術で97.4%の高い割合で,両術式に適切なD3リンパ節郭清が施行されていたことが判明した(表1).術中写真撮影は,手術進行の中断になったり,写真のピンぼけ(評価不能)や撮影の失念などといったことがあるが,手術手技のクオリティコントロール・クオリティアシュアランスの確保には有用であると考えられる.
もう一つの試験遂行の大きな課題は,試験参加同意取得の困難性が挙げられた.当初の試験計画の想定より参加施設からの症例登録が下回ったことに加え,対象集団の主要評価項目(OS)のイベント数が少なかったため,必要症例数が登録中にさらに多く必要となった.本試験では1,000例をこえる症例集積のため,その対策として,患者試験説明・同意取得時に提示する説明動画を作成し説明時に使用することができるようにした,また試験説明・同意取得できなかった症例の理由を試験開始から半年ごとに参加全施設よりアンケート調査を行い,その対策,情報を定期的に会議にて全研究者,試験コーディネーター,試験関係者と共有を行った3).アンケート調査結果からわかったことは,試験に参加することにより施行術式の決定を患者本人ができないことによる試験不参加に加え,腹腔鏡下手術が臨床で増加傾向にあり患者が術式として腹腔鏡下手術を希望する傾向が強いことがわかった.手術手技に関する臨床試験においてその新規術式の手技的安定度と実臨床での普及度のバランスが重要であり,限られたequipoiseのタイミングを念頭においたプロトコール作成,症例登録見込みが必要であることが再認識された.
試験計画立案から登録開始,最終解析結果報告,publishedまで10年以上を要したものの,未解決のクリニカルクエスチョンに回答を導き出す試験であったことに加えて,今後の手術療法の検証するRCTの計画立案,試験遂行の参考となる重要な試験であったと考えられる.

III.JCOG1006試験(No-touch isolation technique:NTITは有用か?)
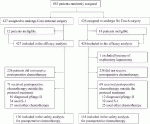
JCOG1106試験は,術前壁深達度SS,SE,SI,A,AIの結腸癌・直腸S状部癌の治癒切除可能病変を対象とし,適切な切除手順を評価する目的で,標準治療である腫瘍部位腸管剥離先行法(Conventional technique)に対して,中枢側血管処理先行法(No-touch isolation technique)の有用性を検証した.これまで,原発巣からのドレナージ静脈を先に結紮する手技は中枢側血管処理先行法(no-touch isolation technique:NTIT)と呼ばれ,大腸癌手術で行われてきた.しかし,この手技による予後への影響に関する臨床的意義についての検証は行われていなかった.JCOG1006試験は853例症例登録のもとRCTが実施された(図4).
本試験では,有効性のprimary endpointとして無病生存期間を設定された.主たる解析結果として,3年無病生存割合は,Conventional technique群で77.3%(95% CI:73.1-81.0%),No-touch isolation technique群で76.2%(95% CI:71.9-80.0%),片側p値=0.59であり,優越性は検証できなかった(図5).また副次評価項目である全生存期間,無再発生存期間,無肝再発生存期間においてもNo-touch isolation technique群の優越性は示せなかった(Takii Y. Ann Surg, 275(5): 849-855, 2022.)4).ネガティブスタディであったが,本研究結果によって,大腸癌手術で未解決であったクリニカルクエスチョンに対して,重要なアンサーを得ることができた.本試験の主解析結果より,腸間膜の完全切除・責任血管の高位結紮に伴うD3郭清,原発巣から適切なマージンを確保した腸管切離によるR0切除が,本邦の実臨床で適切に施行・普及されている現状において,No-touch isolation techniqueは従来の技術に比べて長期予後改善に上乗せするベネフィットをもたらさないことが検証された.
本試験も手術手技のクオリティコントロール・クオリティアシュアランスの確保のため,詳細な手術手技手順を設定することに加えて,術中写真の提出・評価を行っている.詳細なプロトコールのもと,さらにクオリティコントロール・クオリティアシュアランスが確保されている本試験結果は,いち大腸外科医としては想定外の結果であった.おそらく多くの研究者は,No-touch isolation techniqueが有意差を持って良好である結果と,統計学的有意差はないものの生存曲線は上に行っている結果を想定していたと思われる.論文に掲載されている本研究のDiscussionは,No-touch isolation techniqueの優越性が示せなかった考察が記載されておりたいへん納得させられるものであった.

IV.JCOG0212試験(側方郭清は有用か?)
JCOG0212試験は,側方リンパ節腫大(短径で10mm以上)を伴わない腹膜翻転部以下のclinical stage Ⅱ/Ⅲ下部直腸癌患者を対象とし,側方郭清の有用性を検証した.海外と本邦では,下部直腸癌に対する側方リンパ節に対する治療方針が異なり,本邦では,直腸間膜全切除(total mesorectal excision:TME)に側方リンパ節郭清を加えるという手術手技を独自に発展・継承されてきた.本邦では『大腸癌取扱い規約』に側方リンパ節およびその郭清範囲について記載され,その記載に準じて,多くの施設に普及している.本邦オリジナルの側方リンパ節郭清は下部進行直腸癌に対する標準治療として受け入れられてきた.JCOG0212試験は,側方リンパ節郭清の意義を検証するために施行された.
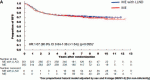
本試験のprimary endpointは無再発生存期間(relapse-free survival:RFS)と設定され,701例が登録,TME単独群とTME+側方リンパ節郭清併用群に割り付けられた(図6).primary endpointである5年無再発生存割合(relapse-free survival:RFS)において,TME単独群が73.3%(95% CI, 68.3%-77.6%),TME+LLND併用群が73.4%(95% CI, 68.5%-77.7%)であり,TME単独群のTME+LLND併用群に対する非劣性は検証されなかった(HR= 1.07,90.9% CI 0.84-1.36,片側P = 0.0547)(図7).局所再発割合がTME単独群で高く,郭清をしなかった側方領域に局所再発が多かったこと,さらに探索的に行った最終解析においても,この結果が再確認された.本邦における下部進行直腸癌に対する標準治療は,従来とかわらずTME+LLND併用であるという結論であった(Fujita S. Ann Surg 2017; 266: 201-207)5).
本試験の主解析結果に加えて,さらに短期成績(ME単独群に比べ,手術時間,出血量は,有意にTME+LLND併用群に多かった.)はLancet Oncolにpublishedされ,海外での高い関心が伺われる試験であった6).

V.今後の展望
大腸癌の長期成績を含めて臨床成績のさらなる向上のためには,手術療法に加えて,術前化学療法,術前放射線療法,術後補助化学療法などの集学的治療法が不可欠である.現在,JCOG1801試験(直腸癌局所再発に対する術前化学放射線療法の意義に関するランダム化比較第Ⅲ相試験),JCOG2006試験(切除可能な局所高度進行結腸癌に対する術前mFOLFOX6療法と術前FOLFOXIRI療法のランダム化第Ⅱ相試験),JCOG2010試験(下部直腸癌に対するtotal neoadjuvant therapy(TNT)およびwatch and wait strategyの第Ⅱ/Ⅲ相単群検証的試験),JCOG2207試験(臨床病期Ⅲの下部直腸癌に対するtotal neoadjuvant therapy(TNT)および選択的側方リンパ節郭清の意義に関するランダム化比較第Ⅲ相試験)が進行中である.うち2試験はTNTストラテジーの有用性を検証する試験である.またJCOG2304試験(進行横行結腸癌に対する縮小手術の意義の検証)が計画立案中である.腫瘍学的根治性とQOL改善を目的とするさらなる臨床試験の結果が待たれる.
VI.おわりに
大腸癌の手術療法の目的はリンパ節郭清を伴う腸管切除である.その目的のためのアプローチ法が,開腹手術か腹腔鏡下手術なのか,リンパ節郭清手技の手順が腫瘍部位腸管剥離先行法(Conventional technique)か中枢側血管処理先行法(No-touch isolation technique)なのか,またTMEに側方リンパ節郭清を追加することが有用なのか,解決すべきクリニカルクエスチョンに対して上記臨床試験より一定の方向性が示された.いずれもトップジャーナルに掲載されているように,クリニカルインパクトは海外においても大きいものであった.手術療法に関する臨床試験では,手術手技のクオリティコントロール・クオリティアシュアランスの確保が重要な因子の一つであり,今後の臨床試験においても上記3試験は大変参考となる試験と考えられる.
利益相反:なし
文献
1) Kitano S , Inomata M , Mizusawa J , et al.: Survival outcomes following laparoscopic versus open D3 dissection for stage Ⅱ orⅢ colon cancer (JCOG0404): a phase 3, randomised controlled trial. Lancet Gastroenterol Hepatol, 2(4): 261-268, 2017.
2) Nakajima K , Inomata M , Akagi T , et al. : Quality control by photo documentation for evaluation of laparoscopic and open colectomy with D3 resection for stage Ⅱ/Ⅲ colorectal cancer: Japan Clinical Oncology Group Study JCOG 0404. Jpn J Clin Oncol, 44(9): 799-806, 2014.
3) Etoh T , Inomata M , Watanabe M , et al.: Success rate of informed consent acquisition and factors influencing participation in a multicenter randomized controlled trial of laparoscopic versus open surgery for stage Ⅱ/Ⅲ colon cancer in Japan (JCOG0404). Asian J Endosc Surg, 8(4): 419-423, 2015.
4) Takii Y , Mizusawa J , Kanemitsu Y , et al.: The Conventional Technique Versus the No-touch Isolation Technique for Primary Tumor Resection in Patients With Colon Cancer (JCOG1006): A Multicenter, Open-label, Randomized, Phase Ⅲ Trial. Ann Surg, 275(5): 849-855, 2022.
5) Fujita S , Mizusawa J , Kanemitsu Y , et al.: Mesorectal Excision With or Without Lateral Lymph Node Dissection for Clinical Stage Ⅱ/Ⅲ Lower Rectal Cancer (JCOG0212): A Multicenter, Randomized Controlled, Noninferiority Trial. Ann Surg, 266(2): 201-207, 2017.
6) Fujita S , Akasu T , Mizusawa J , et al.: Postoperative morbidity and mortality after mesorectal excision with and without lateral lymph node dissection for clinical stage Ⅱ or stage Ⅲ lower rectal cancer (JCOG0212): results from a multicentre, randomised controlled, non-inferiority trial. Lancet Oncol, 13(6): 616-621, 2012.
PDFを閲覧するためには Adobe Reader が必要です。