日外会誌. 125(2): 124-130, 2024
特集
外科におけるRCT―top journalへの道―
5.上部消化管外科におけるRCT―top journalへの道―
|
埼玉医科大学国際医療センター 消化管外科 桜本 信一 |
胃癌術後補助化学療法の臨床試験は1960年代から実施されてきたが,2000年代初頭までは延命効果を証明できるレジメンは確立されなかった.2001年3月初版の胃癌治療ガイドラインで,“多施設共同臨床試験により術後補助化学療法を確立すべきである”とされ,同時期に開始されたACTS-GC試験(Stage Ⅱ/Ⅲ胃癌治癒切除症例に対するS-1 vs 手術単独の第Ⅲ相試験)では,全国109施設から1,059例が短期間に登録された.2006年6月の中間解析で,治療群の有効性と安全性が証明され試験は早期有効中止となり,この結果は胃癌治療ガイドラインで速報された.また,試験結果は2007年NEJMに掲載され,わが国の胃癌術後補助化学療法の標準治療が確立された.
Top journalへRCTの結果を投稿するにあたっては,時代にマッチした治療法を取り入れて多くの患者に有益な研究デザインを立案すること,迅速な症例集積,厳密な統計解析が重要と考えられる.そのためには,外科医,内科医,CRCなど多職種の連携,多施設からの症例登録,クオリティーの高い治療,円滑な試験の実施が最も重要である.本稿ではACTS-GC試験の結果をNEJMへ投稿し,acceptされるまでの経緯を含めて述べる.
キーワード
胃癌, 胃癌術後補助化学療法, ACTS-GC試験, RCT
I.はじめに
胃癌術後補助化学療法は,治癒切除後の微小遺残腫瘍による再発予防を目的としてわが国では1960年代から種々の単剤,多剤併用化学療法の臨床試験が行われてきたが,その有用性を示すエビデンスは構築されなかった.2001年3月初版の胃癌治療ガイドラインでは,「安全にして有効と思われる術後補助化学療法の確立に努力する必要がある」,「多施設共同臨床試験への積極的な取り組みが重要である」と記載され,さらに2004年4月改訂の胃癌治療ガイドライン第2版においても,「治療群(手術+術後補助化学療法)と対照群(手術のみ)の無作為比較対照試験(RCT)を施行する必要がある」とされた.これらから,生存率をEnd Pointとした臨床試験を実施することが急務であった.
ACTS-GC試験1)は,D2郭清を伴ったStageⅡ,Ⅲ胃癌治癒切除症例を対象として術後補助化学療法の有用性を検証するRCTであり,2001年10月から2004年12月までに全国109施設から1,059例が登録され実施された.短期間に多数例が集積されたことは胃癌治療ガイドラインのメッセージを受けて,エビデンスを確立することへの外科医の気運が高まったものと考えられた.2006年6月の中間解析で治療群は手術単独群に対して有効性と安全性が証明され,試験は早期有効中止となり胃癌治療ガイドラインで速報された2).ACTS-GC試験結果は“Adjuvant Chemotherapy for Gastric Cancer with S-1, an Oral Fluoropyrimidine(経口フッ化ピリミジン系薬剤S-1を用いた胃癌に対する補助化学療法)”のタイトルでThe New England Journal of Medicine(NEJM)に投稿され,2007年11月1日号に掲載された.これによりわが国の胃癌術後補助化学療法の標準治療が確立された.約20年前を回顧しながら,論文の構想,投稿から掲載まで,掲載後の反響などについて述べる.
II.研究の背景
わが国の胃癌術後補助化学療法は1960~1970年代は手術単独群を対象とした試験が中心に行われたが,ほとんどの試験で術後補助化学療法の有用性は証明されなかった.ただし,後層別解析により一部で有用性が認められた.1970年代後半~1980年代は化学療法同士を比較した試験が中心で,層別解析では一部に有用性が認められたが標準的な治療法は見出せなかった.これまでの試験は,サンプルサイズが過少,割付法(封筒法によるBias等),データ解析の問題点(後層別解析による有効性の証明),外科手術のクオリティーコントロールの問題など,手術単独群と比較した質の高い試験が不在であった(図1).そこで,1980年代後半からは,日本臨床腫瘍研究グループ(JCOG)の胃がんグループが中心となって手術単独をコントロールとした大規模PhaseⅢ試験(JCOG8801,JCOG9206-1,2)3)が実施された.しかし術後補助化学療法の有用性は示されなかった.これは日本の手術単独群の治療成績が優れていること,および薬剤強度不足によるものと考えられた.
一方,米国を中心に実施されたINT0116試験4)では,胃癌・食道胃接合部腺癌症例を対象として,手術単独群と放射線化学療法群(手術単独vs 5-FU/RT)の生存期間が比較検討され,治療群で有意な生存期間の延長が認められ術後放射線化学療法の有用性が証明された.また,英国を中心に実施されたMAGIC試験5)では,胃癌・食道胃接合部腺癌症例を対象として,手術単独群と術前・術後化学療法群(手術単独 vs 術前術後ECF)が検討され,治療群において有意な生存期間の延長が認められ術前術後化学療法の有用性が証明された.しかし,INT0116試験では,D2郭清が10%,D1が36%,D0が54%で,手術単独の3年生存率が41%,MAGIC試験ではD2が41.4%,D1が19.5%,D0が15.1%,食道癌が24%含まれ,手術単独群の5年生存率は23%であった.わが国と海外では手術の手技(特にD2郭清率)が大きく異なり,海外での対照群(手術単独群)の生存率は低かった.また,術前・術後の放射線療法実施などわが国とは治療戦略が異なることから,この結果をそのまま本邦に適用するのは適切ではなく,日本には日本の治療にあったエビデンスが必要と考えられた.1999年にわが国で薬事承認されたS-1は,進行再発胃癌に対して単剤で40%以上の奏効率が得られ6),その効果が期待されてACTS-GC試験での治療群として採用された.

III.試験デザインと結果
・試験デザイン
ACTS-GC試験は,治癒切除(D2郭清)を受けたStageⅡ,Ⅲ症例を対象として胃癌術後補助化学療法の有用性を検証するRCTであり,主要評価項目は全生存期間,副次的評価項目は無再発生存期間および術後S-1投与の安全性であった.本試験は対照群(手術単独群)の5年生存率を70%と仮定し,S-1群の全生存期間のハザード比が0.70(この場合S-1投与群の5年生存率は77.9%)となることを検証する優越性試験としてデザインされ(図2),追跡期間を登録終了5年間として各群500例,計1,000例の登録が必要とされた.また,中間解析を登録完了後,1年と3年で実施することが計画された.
・症例登録と結果
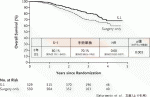
2001年10月から2004年12月に1,059例が登録され,治療群(S-1群)529例,手術単独群が530例であった.無作為割り付け後,25例(治療群14例・手術単独群11例)が不適格であることが判明した.第1回中間解析が,登録終了1年後(2005年12月)の追跡データにより2006年6月に実施され,全生存期間・無再発生存期間のいずれも治療群で良好な結果であった(図3).中間解析の早期中止基準はp=0.0011と設定されており,効果・安全性評価委員会より試験の早期有効中止が勧告された.

IV.投稿論文の構想
・論文執筆担当と投稿先
本試験のプロトコールでは最も多くの症例を登録した施設が論文執筆の権利を有する取り決めになっており,最多登録施設の北里大学東病院(私の前勤務病院)が論文執筆を担当することになった.また,共著者は試験調整委員,アドバイザー,生物統計家および症例登録数上位10施設の施設責任医師とすることが決められていた.本試験は全国109施設が参加し,多くの医師,コメディカルの協力により得られた結果であり,可能な限りレベルの高い雑誌を目指し,世界で最も権威のある医学雑誌NEJMに投稿することとなった.
・論文の構想
本試験は中間解析結果で有効と評価され早期公表となったため,速やかに論文を投稿して掲載される必要があった.日本では標準的にD2郭清が行われているが,欧米で行われている郭清度と異なるため,日本のみで実施された試験結果がNEJMに受け入れられるよう,以下の点に留意して論文を作成した.
1)論文作成時には,すでに米国と欧州でそれぞれ実施された臨床試験で胃癌手術の補助療法の有効性を示した結果4)
5)がNEJMに掲載されていたため,これら欧米の臨床試験との違いを明確にして新規性をもたせること.
2)中間解析における統計手法と結果の評価について理解しやすい記載にすること.
3)欧米の主要な癌関連雑誌と比較して本文の単語数に制約があり,簡潔にまとめること.
欧米の臨床試験との違いに関しては,リンパ節郭清の違いが最も重要な要因であった.D0またはD1郭清が実施されている欧米の臨床試験結果に対して,日本ではD2郭清が実施され,同じ胃癌手術例でも試験の対象が異なることを述べた.D2郭清を標準としている日本および東アジアの手術成績は欧米のそれと比較して優れており,欧米の補助療法を付加したグループにおいても日本のD2郭清後の生存率に達していなかった.このためD2郭清をベースとしたわれわれの結果は,より説得力のあるものと考えていたが,本論文がリンパ節郭清に関する議論になることは好ましくないことや単語数の制約もあり,リンパ節郭清の手術成績に関する考察は避け,あくまでも対象が異なることのみ述べることとした.
統計関連項目については,臨床家が正確に記載することは難しく,特に本臨床試験は中間解析結果で有効と評価され結果の公表に至ったため,中間解析に関する統計手法等の詳細な記載が不可欠であり,生物統計家に解析を委ねた.投稿論文の規程(本文の単語数,アブストラクトの単語数,図表枚数,引用文献数などの制限)では,癌関連で欧米の主要な雑誌の本文の単語数3,000語以内に対してNEJMは2,700語以内であり,本文を要領よくまとめなければならなかった.このため,英文を正確かつ簡潔に記載することが重要であり,医学論文の英文チェックに慣れた専門家にお願いした.
V.論文投稿から掲載まで
・投稿時~査読結果入手まで
共著者全員の確認を経て,NEJMに投稿した.Webでの論文投稿後,まずNEJMからの連絡メールが施設サーバーで誤って迷惑メールの扱いになっていないか確認した.その後,PaperTRAILで投稿論文が受領後,間もなくレビューワーに送られたことが確認でき,門前払いされることなく査読にまわったことで安心した.PaperTRAILではレビューワーからの回答状況(受領の有無)について確認することができ,適時PaperTRAILを見ることで査読結果の連絡時期の見通しが立った.
・査読結果対応~再投稿まで
投稿から1カ月ほどでエディターから査読結果をメールで受け取った.3名のレビューワーからは,総評として好意的なコメント(よくデザインされた試験,説得力のある結果,日本などで多くの命が救われるであろう)が届き,投稿前に日本のみで実施された試験結果が受け入れられるか不安であったが払拭された.個別の指摘事項として,統計家と思われるレビューワーから再解析(生存期間の起算日を手術日ではなく割付日とすべき)の指摘があり,エディターもこの指摘に関して完全に同意するとのコメントが付記されていた.手術後6週間以内に割付を行うことになっていたので,起算日の変更が試験結果に影響することはほとんどないと思われたが,エディターが同意している以上対応せざるを得なかった.生存率成績が手術後でなく割付後生存率となることに関して,臨床的な意味合いに疑問を持った共著者もいたが,ランダム化試験として正論の指摘であり再解析して対応した.共著者の疑問は臨床家として妥当であり,考察に手術日を起算日とした生存率(3年生存率)とハザード比を記載して,割付日を起算日とした結果と同様であることを追記した.また,別のレビューワーからは,欧米との手術成績の違いとS-1の毒性が北米と日本や東アジアで異なる(北米で高くみられている)ことから一般化には限界があり,アブストラクトの結論で限定すべきとの指摘があり「東アジアの患者に対して有効な治療」とした.
・再投稿~アクセプトまで
再解析後に改訂した論文について,共著者の確認を経て査読結果受領から1カ月後に再投稿することができた.再投稿後,エディターから何度かメールで確認事項などの問い合わせがあり,その都度対応したがPaperTRAILを見る限り再投稿後にレビューワーに送られた形跡はなかった.
・アクセプト~掲載まで
アクセプトの連絡はメール(非公式:公式には後日郵送されたレター)で受け取った.投稿した論文が原稿編集部門に回され,以降は原稿編集部門の編集担当者からのメールに対応することとなった.この時のメールに添付された“Embargo Guidelines”に掲載されるまでの規制事項があり,掲載されるまでアクセプトされたことも含めて情報の取り扱いに注意した.その後,確認のためのゲラ刷り(galley proofs)が送付される時期(週)が連絡されてきたので,スケジュールに入れておくことができた.
予めゲラ刷りが送付される時期についての連絡は受けていたが,忘れかけていた週末(金曜日)の朝にメールで多数(80以上)のクエリ付きのゲラ刷りが送られてきた.このメールには,翌週の火曜日の午前中(米国東部時間)までに編集担当者に電話して回答するように(電子ファイルを送付しないよう)との記載があった.なお,翌日のメールで日米間の時差を考慮してメールでの回答でも構わないとの連絡があったが,論文のネイティブチェックをお願いした先生にサポートしていただき電話で回答することにした.幸い休日を挟んだので,多数のクエリの確認と編集担当者への回答準備を行うことができた.クエリの多くは原稿編集部門で書き直した英文の確認であった.全世界の読者に共通の理解が得られるよう,用語や表現についてはNEJMの標準に統一されているようであり,論文作成者の意図と齟齬がないようディスカッションしたいとのことであり,メールではなく電話での回答を求めた理由が理解できた.
掲載予定の4週間前に掲載号の連絡と最終のゲラ刷りの確認があり,この時は24時間以内に回答(メール)する必要があった.また,この回答後も数回メールで確認を求められた.再投稿以降のエディターや編集担当者からのメールによる確認は,日々の診療の中で対応することは結構大変であった.特に掲載が近くなるにつれて,回答期限も短くなり,メールのチェックは欠かせなかったが,本試験は製薬会社共催であったため学術担当者の協力が得られ大変助けられた.
VI.掲載後の反響
胃癌はわが国で最も罹患数の多い癌腫の一つであり,有効な補助化学療法を確立することは重要なテーマであった.本試験の結果は,学会発表やメディアを通じて多くの医師が知るところであったが,NEJMへの掲載により胃癌治療ガイドライン(2008年2月速報版2))で「胃癌術後補助化学療法としてのS-1投与は安全にして有効であり,StageⅡ,Ⅲ胃癌手術後の標準治療としてよい」と評価され標準治療として位置づけられた.
VII.おわりに
ACTS-GC試験の結果が,NEJMへ掲載されるまでの経緯を述べた.近年,免疫チェックポイント阻害剤や分子標的薬の開発はめざましく,有効な癌化学療法が数多く確立されてきた.一方,癌が発生する限り病巣の切除は外科医の使命であり,化学療法後の難度の高い手術を安全に執刀できる技量を身に着けるための外科的修練は,今後も益々重視されるであろう.外科手術は,開腹・開胸術から腹腔鏡下手術,ロボット支援下手術へと発展してきた.最新の手術機器を使いこなし精緻でQOLの良好な手術を提供して,多くの患者に有益な治療法を開発することが次世代の外科医の課題と思われる.そして,その結果を世界のtop journalへ発信し,日本の外科学発展に寄与していただきたいと願っている.
利益相反:なし
文献
1) Sakuramoto S , Sasako M , Yamaguchi T , et al.: Adjuvant chemotherapy for gastric cancer with S-1, an oral fluoropyrimidine. N Engl J Med, 357: 1810-1820, 2007.
2) 日本胃癌学会ホームページ.2008年2月. http://www. jgca.jp/guideline/index.html
3) Nashimoto A , Nakajima T , Furukawa H , et al.: Fluorouracil, and Cytosine Arabinoside followed by oral Fluorouracil in serosa-negative gastric cancer:Japan Clinical Oncology Group 9206-1. J Clin Oncol, 21:2282-2287, 2003.
4) Macdonald JS , Smalley SR , Benedetti J , et al.:Chemotherapy after surgery compared with surgery alone for adenocarcinoma of the stomach or gastroesophageal junction. N Engl J Med, 345:725-730, 2001.
5) Cunningham D , Allum WH , Stenning SP , et al.: Perioperative chemotherapy versus surgery alone for resectable gastroesophageal cancer. N Engl J Med, 355: 11-20, 2006.
6) Koizumi W , Kurihara M , Nakano S , et al.: Phase II study of S-1, a novel oral derivative of 5-fluorouracil, in advanced gastric cancer. Oncology, 58: 191-197, 2000.
PDFを閲覧するためには Adobe Reader が必要です。