日外会誌. 123(3): 286-293, 2022
会員からの寄稿
多機関共同後ろ向き研究における研究デザインと人材育成:京都食道胃手術勉強会での取り組み
|
1) 京都大学医学部附属病院 消化管外科 藤田 悠介1) , 錦織 達人1) , 下池 典広1) , 村上 克宏1) , 門川 佳央2) , 伊丹 淳3) , 近藤 正人4) , 金谷 誠一郎5) , 川田 洋憲6) , 畑 啓昭7) , 山本 道宏8) , 金城 洋介9) , 田中 英治10) , 間中 大11) , 佐藤 誠二12) , 岡部 寛13) , 山下 好人14) , 姜 貴嗣15) , 後藤 禎人16) , 中山 健夫16) , 川上 浩司17) , 田中 司朗18) , 久森 重夫1) , 角田 茂1) , 肥田 侯矢1) , 小濱 和貴1) |
多機関共同後ろ向き観察研究はリアルワールドの知見を得られる有用な研究手法であるが,臨床疫学的原則に基づくバイアスの制御が必要である.当教室では外科関連施設や社会健康医学系専攻の専門家と協力し,若手外科医主導で研究を実施してきた.多機関共同後ろ向き観察研究の研究デザインの要点,研究を支える実施体制と人材育成に関して紹介する.
キーワード
多機関共同研究, 後ろ向き観察研究, 研究デザイン
I.はじめに
ランダム化比較試験(RCT)は,未測定や未知の交絡を調整でき,外科領域でも介入の有効性を評価する上で有用な研究手法である.しかし,適切なサンプル数を有するRCTの研究資金は高額で,患者登録に時間を要し,実験的条件下で実施されるため結果の一般化可能性に乏しいといった欠点を有する.多機関共同後ろ向き観察研究(令和3年・人を対象とする生命科学・医学系研究に関する倫理指針で複数の研究機関で実施する研究を「多施設」ではなく「多機関」と呼称)は,比較的安価で短期間にリアルワールドの知見を得られる研究手法である1)2).しかし,複数の施設から後ろ向きに情報を収集した場合,様々な背景を有する患者や治療方法が混在するため,バイアスの発生リスクが高くなる3).データ収集後にバイアスを制御することは難しく,データを収集する前に,研究疑問を明確にし,「研究デザイン」を固める必要がある4).質の高い観察研究の結果は,RCTの結果と似ることが複数のシステマティックレビューから示されている5)
~
8).
京都食道胃手術勉強会:Kyoto Esophageal Gastric surgery study Group(KEGG)は,京都大学外科関連の15施設が参加する手術手技勉強会で,2年間で三つの研究テーマに関して多機関共同後ろ向き観察研究を実施してきた.その研究デザインの作成方法と研究を支える人材育成について報告する.
II.多機関共同後ろ向き研究の研究デザイン作成方法
多機関共同後ろ向き観察研究の研究デザイン方法を三つに分けて概説する.研究デザインが決定された後にデータ収集や解析を行うことが重要である.
1.臨床疑問から研究疑問への構造化
臨床を行っていれば,自院や他院の診断や治療方法に疑問を生じることがある.例えば,胃癌治療ガイドラインで進行胃癌に対しての標準手術は開腹手術とされているが,比較的進行度の高い肉眼型4型胃癌に対して腹腔鏡手術を行っている施設もあり,「4型胃癌に腹腔鏡手術を行うことは妥当か」といった疑問が生じる.それらを明らかにする研究を開始するためには,第一に臨床疑問を研究疑問に構造化する必要がある.
網羅的な文献検索を行い,研究を行う背景として,これまで何が分かっていて,何が分かっていないのか(What is known or unknown)を整理する.そして,分かっていないことを解明するため,誰を対象に(Patient:対象者),何を調べたいのか(Exposure:暴露要因),それは何を対照として(Comparison:比較対照),どの結果への効果を調べたいのか(Outcome:評価項目)を定義する9).
それぞれの頭文字をとったPECO(ペコと呼ばれる.Intervention:介入要因の場合はPICOピコと呼ばれる.)の形式に先程の臨床疑問を構造化すると以下の通りである.
P:4型胃癌に対して胃癌手術が行われた患者
E:腹腔鏡下手術
C:開腹手術
O:全生存期間
他の臨床疑問の例として,「胃癌に対する腹腔鏡下胃全摘術における最適な食道空腸吻合は何か」を考えてみる.以下のように,調べたい疾患対象,手術方法,アウトカムを明確にすることで,臨床疑問を研究疑問に昇華させることがきる.
P:食道浸潤長が3㎝以内の胃癌に対して腹腔鏡下胃全摘術が行われた患者
E:linear staplerによる食道空腸吻合
C:circular staplerによる食道空腸吻合
O:吻合部関連合併症:Clavien-Dindo分類GradeⅢa以上の術後30日以内の縫合不全もしくは吻合部出血,術後1年以内の吻合部狭窄
2.バイアスの制御
構造化された研究で調べたいことは,ExposureとOutcomeとの関係性にあるが,その関係性を歪ませるバイアスをデータ収集前に十分に検討する必要がある.バイアスは,交絡,選択バイアス,情報バイアスに一般的に分類される10).
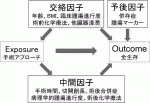
交絡因子がExposure群とComparison群のどちらかに偏っていれば,2群を比較しても,Outcomeへ影響を与えたのが背景の差異か暴露要因による差異か判定できない.調べたいExposureとOutcomeとの関係性を誤って解釈しないように,交絡因子の偏りを調整する必要がある.まず,背景知識や先行研究からExposureやOutcomeに影響を与える交絡因子,中間因子,予後因子などの第3の因子11)をリストアップし,概念図にまとめる(図1).Outcomeに影響する因子が予後因子で,その中でExposureと関連する因子が交絡因子である.ExposureとOutcomeの中間に位置する因子が中間因子で,中間因子は統計解析で調整してはならない.腹腔鏡手術と開腹手術の長期予後を比較する4型胃癌の研究を例にすると,術前の腫瘍マーカー値は予後因子,腫瘍進行度は交絡因子,切開創長は中間因子となる.
交絡因子の調整方法は成書に譲るが,対象集団の限定(Restriction)や,多変量解析/傾向スコア法といった統計学的手法が存在する12)13).4型胃癌の研究を例にすると,手術アプローチ選択や長期予後に影響を与える他臓器浸潤を除外基準にすることで,交絡因子の影響を制御することができる.ただし,解析対象を限定すると,研究結果の一般化可能性が低下し,除外した母集団には結果を直接外挿できないことに注意が必要である.また,統計学的手法を用いることで,データ解析時に交絡調整することができるが,事前に交絡因子を想定しデータ収集していないと,解析で調整することはできない.
選択バイアスや情報バイアスの詳細についても成書に譲るが,注意すべきは,データ収集後では統計学的手法を用いてもバイアスを制御できないことである.選択バイアスは研究対象者を選定する段階で生じるバイアスであるが,例えば母集団を反映しない,特殊な患者集団からデータ収集しても,研究結果を一般患者に応用することはできない.また,情報バイアスとはそれぞれの因子を測定する際に生じるバイアスのことであり,誤分類されたデータを収集してしまうと,研究結果は信頼されるものではなくなる14).胃癌の取り扱い規約を例に挙げると,様々なバージョンの規約から定義されたカルテ上の腫瘍進行度をそのまま収集しないように,データ収集するために使用する規約を事前に定義する必要がある.
また,外科領域における観察研究では,手術手技のQualityへの考察が必須である.例えば,熟練外科医が片群だけに偏っていれば交絡因子になり得るし,D2郭清と定義した手術で郭清が不十分であれば情報バイアスになりえる.KEGGでは,全施設で日本内視鏡外科学会技術認定医が腹腔鏡手術の参加,指導にあたり,2005年からビデオクリニックを通じて手術手技の洗練と標準化に取り組んでいる.研究対象となる全ての手術Qualityを保証する手段は確立していないが,日常の手術手技のQuality向上への試みが,多機関共同後ろ向き研究におけるQuality Controlとして肝要である.
3.臨床・研究の専門家との協同
単施設での後ろ向き研究では,自施設の症例数,Exposure群とComparison群の比率,各治療方法の変遷,適応基準などについて,漠然としても知識があり,それらをもとに研究疑問をたてることが可能である.しかし,それらを知り得ない多機関共同研究では,研究疑問と実際得られる情報が乖離するリスクが存在し,特に過去の症例に遡る後ろ向き研究で大きくなる.例えば,Exposure群,Comparison群のどちらか片群が極端に少なければ,妥当な比較は困難である.多機関共同後ろ向き観察研究を実施する際には,各施設の状況についてアンケートを取るなどし,サンプル数,治療変遷からの両群比率,イベント数などを推定し,妥当な比較研究の実現可能性を検討することが求められる.
また,研究疑問や交絡因子の臨床的妥当性についても,多施設の臨床専門家や研究専門家からレビューを受けることは重要である.臨床疑問の段階から多施設ミーティング等で研究素案を発表し,批判的吟味を得ることで,研究疑問をより洗練させ,解析時に必要な交絡因子を同定することができる.更に,生物統計家や臨床疫学研究専門家が参画することで,研究デザインや統計解析手法の妥当性がより高まる.
例えば,適切なサンプル数を決定するためには,Exposure群とComparison群の差の大きさやばらつきなどについて文献検索やアンケートから見積もりを立て,各専門家で合意を得ておく必要がある.通常,両群の差が小さかったり,ばらついたりしている場合には,大規模なサンプル数が必要になる.十分なサンプル数がない研究では,本当は差があるのに差がないと結論してしまう過誤が発生する確率が高くなる.「観察的疫学研究報告の質改善のための声明(STROBE声明)」では,研究者はサンプルサイズを決定した思考プロセスを提示すべきであるとされている.比較的稀な疾患などで実現可能なサンプルサイズが決められてしまう場合もこれに当てはまる15)16).こうしたプロセスは,仮に得られた結果が「P ≤ 0.05」の有意水準を満たさなかったとしても,Positive,Negativeの機械的な二分類を超え,効果の大きさなど科学的な考察を行うことにも寄与する17)18).
そして,研究の対象患者,交絡因子,サンプル数などを決定した多施設間の事前アンケートやミーティングなどのプロセスを論文に明示することで,比較の妥当性をレビューワーや読者に適切に伝えることができる.このように多機関共同後ろ向き研究の研究デザインを作成するためには,中核施設だけの検討だけでなく,各専門家が協同できる体制作りが求められる.
III.KEGGで実施した多機関共同後ろ向き研究
研究1.4型胃癌に対する腹腔鏡下手術の妥当性を検討した研究19)
事前アンケートを通してサンプルサイズを概算し,2005年から2015年に胃切除を受けた4型胃癌患者を対象とし,全生存期間に関して,腹腔鏡手術(n=62)と開腹手術(n=226)を比較した.患者背景や腫瘍学的因子を調整した多変量解析のハザード比で,両群に有意差を認めなかった(HR=0.98,95%CI=0.63-1.43).上記の結果から,4型胃癌に対する腹腔鏡下手術は予後の悪化と関連しているとは言えないとした.
研究2.腹腔鏡下胃全摘術の食道空腸吻合におけるlinearとcircular staplerの比較を行った研究20)
2010年から2016年に腹腔鏡下胃全摘術を受けた患者を対象に,Clavien-Dindo分類でGradeⅢ以上の吻合部関連合併症(縫合不全,吻合部出血,吻合部狭窄)に関して,食道空腸吻合をLinear Staplerで行った群(n=605)とCircular Staplerで行った群(n=224)を比較した.傾向スコアmatchingを行った後,吻合部関連合併症はLinear stapler群で4.1%,Circular stapler群で11.7%(p=0.008)と前者で有意に少なかった.上記の結果から,腹腔鏡下胃全摘術の食道空腸吻合におけるLinear Staplerを用いた吻合はCircular staplerを用いた吻合よりも安全であるとした.
研究3.実臨床下でのロボット支援下胃切除の安全性の検討を行った研究(Gastric Cancer Accepted)
2017年から2019年にロボット支援下胃切除を受けた患者(n=336)を対象とし,Clavien-Dindo分類でGradeⅡ以上の術後合併症を評価した.この研究で術後合併症割合は14.9%であった.先進医療で行われた先行研究(保険償還前で術者や進行度に制限があるもの)の合併症割合は21.2%21)であり,上記の結果から,ロボット支援下胃切除術は実臨床下においても安全に行われていたとした.
以上の3研究の概要を表1に示す.

IV.多機関共同後ろ向き研究を支える人材育成と展望
外科領域でExposureとOutcomeとの因果関係を検討するには,臨床知識に加えて,ある一定の研究に関する専門的知識が必要になる.KEGGでは,臨床経験に基づく臨床疑問を持つ卒後7~10年程度の若手外科医に,大学院への進学と京都大学大学院医学研究科社会健康医学系専攻(School of Public Health;SPH)が提供する臨床研究者養成コース(Master of Clinical Research:MCR)の履修を推奨している.MCRは1年間の特別プログラムで,生物統計,研究デザイン,臨床疫学,医療経済などを座学と実習で学ぶ.
MCRでの座学・実習と並行して,各大学院生は主たる研究テーマを1~2年かけて決定する.研究デザインの立案にあたっては,外科学講座教官やSPH教官から,多機関共同研究の実施にあたっては施設指導医からまたは各種ミーティングで指導を得る.KEGGでは新型コロナ感染症の流行期には変動があったものの,webミーティングシステムを利用して,概ね3カ月毎に研究ミーティングを行っている.各大学院生は自身の研究を主導的にマネージメントするとともに,他の臨床疫学研究にも複数従事して,データ収集,クリーニング,解析,論文作成のスキルをOn-the-job trainingで深める.データ収集の際には当該施設の倫理委員会等の許可を得て,多忙な外科医をサポートし,3年次にはデータ解析の終了,4年次には論文執筆と博士(医学)の取得を目標としている.
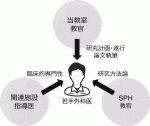
多機関共同の前向き介入研究や治験を実施するためには,多大な資金や研究期間が必要で,若手外科医が主導することは通常困難である.しかし,当会では臨床経験とリサーチマインドのある若手外科医が,グループ全体のサポートを受け,臨床業務フリーに臨床疫学研究手法を学ぶ時間と環境を得て,多機関共同後ろ向き観察研究を主導してきた.これらの経験を経た若手外科医が臨床に復帰することで,更にグループ内の多機関共同研究が活性化し,外科治療と臨床研究のスキルを高め,国内外施設との共同研究にも貢献していくことができるものと考えている.KEGGにおける多機関共同研究を支える人材育成についての概要を図2にまとめた.
V.おわりに
KEGGで実施してきた多機関共同後ろ向き研究の研究デザインの作成方法と研究を支える人材育成について概説した.現在,多機関共同のオンライン臨床データベースを構築し,より系統的なデータ収集に取り組んでいる.今後も臨床と研究の両分野からアプローチすることで,より質の高いエビデンスの創出に貢献していきたいと考えている.
また,京都大学SPH,MCR(http://sph.med.kyoto-u.ac.jp/)は,全国・世界中の研究者・医療職・臨床医に門戸が開かれている.その他,臨床疫学研究手法を学ぶ機会としては,国内外のSPH,成書,日本臨床疫学会(http://www.clinicalepi.org/)やQOL-PRO研究会(http://qol_pro.umin.jp/)といった学会・研究会など多様に存在する.全国のリサーチマインドのある若手外科医が,臨床疫学研究についての学びの機会を得て,自らの臨床経験に基づく疑問を解決する力を身に着け,外科領域の臨床疫学研究に従事することが期待される.それにより,外科治療に関する本邦の多機関共同の臨床疫学研究が更に活性化し,世界の外科治療の発展に貢献していくものと考えられる.
本論文の要旨は,2021年4月に開催された第121回日本外科学会定期学術集会で発表した.
利益相反:なし
文献
1) Black N: Why we need observational studies to evaluate the effectiveness of health care. BMJ, 312(7040): 1215-1218, 1996.
2) 肥田 侯矢:【臨床試験デザイン】外科領域の臨床研究 臨床医の視点から.日外会誌,117(1): 28-32, 2016.
3) Higgins JP, Green S: Cochrane Handbook for Systematic Reviews of Interventions:Cochrane Book Series:John Wiley and Sons, pp1-649, 2008.
4) 福原 俊一:デザインが研究の質を決定する.麻酔,68(増刊):S188-S195, 2019.
5) Anglemyer A, Horvath HT, Bero L: Healthcare outcomes assessed with observational study designs compared with those assessed in randomized trials. Cochrane Database Syst Rev, 2014(4):MR000034, 2014.
6) Concato J, Shah N, Horwitz RI: Randomized, controlled trials, observational studies, and the hierarchy of research designs. N Engl J Med, 342(25): 1887-1892, 2000.
7) Hoshino N, Fukui Y, Hida K, et al.: Similarities and differences between study designs in short- and long-term outcomes of laparoscopic versus open low anterior resection for rectal cancer:A systematic review and meta-analysis of randomized, case-matched, and cohort studies. Ann Gastroenterol Surg, 5(2): 183-193, 2021.
8) Hoshino N, Sakamoto T, Hida K, et al.: Difference in surgical outcomes of rectal cancer by study design:meta-analyses of randomized clinical trials, case-matched studies, and cohort studies. BJS open, 5(2):zraa067, 2021.
9) Vandenbroucke JP, von Elm E, Altman DG, et al.: Strengthening the Reporting of Observational Studies in Epidemiology (STROBE):explanation and elaboration. Int J Surg, 12(12): 1500-1524, 2014.
10) Grimes DA, Schulz KF: Bias and causal associations in observational research. Lancet, 359(9302): 248-252, 2002.
11) 福原 俊一:臨床研究の道標-7つのステップで学ぶ研究デザイン.健康医療評価研究機構,2017.
12) Psaty BM, Siscovick DS: Minimizing bias due to confounding by indication in comparative effectiveness research:the importance of restriction. JAMA, 304(8): 897-898, 2010.
13) Ranstam J, Cook JA: Causal relationship and confounding in statistical models. Br J Surg, 103(11): 1445-1446, 2016.
14) Althubaiti A: Information bias in health research:definition, pitfalls, and adjustment methods. J Multidiscip Healthc, 9: 211-217, 2016.
15) Vandenbroucke JP, von Elm E, Altman DG, et al.: Strengthening the Reporting of Observational Studies in Epidemiology (STROBE):explanation and elaboration. Epidemiology, 18(6): 805-835, 2007.
16) Vandenvbroucke JP, von Elm E, Altman DG, et al. (福原俊一,山口拓洋,山崎 新,他・監訳):観察的疫学研究報告の質改善(STROBE)のための声明─解説と詳細─.2021年1月31日. https://www.strobe-statement.org/fileadmin/Strobe/uploads/translations/STROBE-Exp- JAPANESE.pdf
17) 佐藤 俊:ASA声明と疫学研究におけるP値.計量生物学,38(2): 109-115, 2018.
18) Wasserstein RL, Lazar NA: The ASA Statement on p-Values:Context, Process, and Purpose. The American Statistician, 70(2): 129-133, 2016.
19) Fujita Y, Nishigori T, Kadokawa Y, et al.: Comparative Outcomes of Laparoscopic Gastrectomy and Open Gastrectomy for Scirrhous Gastric Cancer:A Multicenter Retrospective Cohort Study. Ann Surg Open, 2(2):e063, 2021.
20) Murakami K, Obama K, Tsunoda S, et al.: Linear or circular stapler? A propensity score-matched, multicenter analysis of intracorporeal esophagojejunostomy following totally laparoscopic total gastrectomy. Surg Endosc, 34(12): 5265-5273, 2020.
21) Uyama I, Suda K, Nakauchi M, et al.: Clinical advantages of robotic gastrectomy for clinical stage I/II gastric cancer:a multi-institutional prospective single-arm study. Gastric Cancer, 22(2): 377-385, 2019.
PDFを閲覧するためには Adobe Reader が必要です。