日外会誌. 121(4): 417-422, 2020
特集
食道癌診療の現況と展望
3.診療アルゴリズム
|
慶應義塾大学医学部 一般・消化器外科 川久保 博文 , 北川 雄光 |
食道癌治療ガイドラインは2002年に初版として発刊され,2017年6月に発刊された第4版は,名称を食道癌診療ガイドラインに変え,エビデンス至上主義からより実際の医療に役立つ判断を取り入れた最新のガイドラインとして発刊された.食道癌の治療方針は原則として食道癌診療ガイドラインに記載されている食道癌治療のアルゴリズムおよびアルゴリズムに基づいた治療方針に従って決定することが推奨されている.
食道癌は疾患特異的な問題点が多くあり,画一的な治療法を決定することは困難である.そのため,その患者の様々な情報を総合的に考慮したうえで治療方針を決定されなければならない.食道癌は高齢者に多く発生するため,併存疾患や機能障害を有している患者が多く,その患者の進行度に対する標準治療ができないことが多い.そのため,個々の患者の状態を考慮に入れなければならない.治療法としては内視鏡治療,手術,化学療法,放射線療法を組み合わせた集学的治療が行われるが,早期癌から進行癌に至るまで多くの治療法が適応となり,その組み合わせ,順序を含めると治療の選択肢が多岐にわたる.一方で胃癌,大腸癌,乳癌,肺癌などと違い,症例数が多くないため,大規模な臨床研究を施行することが困難であり,信頼度の高いエビデンスが得られ難い.本稿では食道癌診療ガイドラインにおける進行度別のアルゴリズムを示し,進行度別の治療方針を概説する.
キーワード
食道癌, 手術, 集学的治療, アルゴリズム, 食道癌診療ガイドライン
I.はじめに
近年の内視鏡検診の普及や,ハイビジョン内視鏡やヨード染色の普及,narrow-band imaging(NBI)システム,拡大内視鏡などの内視鏡診断の進歩により,多くの早期食道癌が発見されるようになった.また,進行癌に対してもEUS,ヘリカルCT,MRI,PET検査などの画像診断の進歩によって,隣接臓器への浸潤,リンパ節転移や遠隔転移診断がより精密に行われている.食道表在癌に対しては,Endoscopic mucosal resection(EMR)やEndoscopic submucosal dissection(ESD)を中心とした内視鏡治療が進歩し,わが国の早期食道癌の診断・治療は世界をリードしている.一方で手術治療は1980年代に3領域リンパ節郭清を伴う食道切除が開始され,最近では手術手技および周術期管理が確立されたものとなり,欧米を凌駕する手術成績をあげている.しかしながら,手術治療単独治療の成績はこれ以上の飛躍的な向上は望めない状況であった.わが国の食道癌の90%以上を占める扁平上皮癌は化学療法や放射線療法に感受性が高く,食道癌手術治療成績のさらなる向上のためには,化学療法,放射線療法を組み合わせた集学的治療が不可欠と考えられている.
食道癌治療ガイドラインは2002年に初版として発刊され,その後診断に関する記載が追加され,食道癌診断・治療ガイドラインとして2007年,2012年と5年ごとに改定された.2017年6月に発刊された第4版は,名称を食道癌診療ガイドラインに変え,エビデンス至上主義からより実際の医療に役立つ判断を取り入れた最新のガイドラインとして発刊された1).食道癌の治療方針は原則として食道癌診療ガイドラインに記載されている食道癌治療のアルゴリズムおよびアルゴリズムに基づいた治療方針に従って決定することが推奨されている.
本稿では食道癌診療のアルゴリズムを概説する.
II.食道癌の治療方針を決定するために必要な情報
食道癌は疾患特異的な問題点が多くあり,画一的な治療法を決定することは困難である.そのため,その患者の様々な情報を総合的に考慮したうえで治療方針を決定されなければならない.食道癌は高齢者に多く発生するため,併存疾患や機能障害を有している患者が多く,その患者の進行度に対する標準治療ができないことが多い.そのため,個々の患者の状態を考慮に入れなければならない.治療法としては内視鏡治療,手術,化学療法,放射線療法を組み合わせた集学的治療が行われるが,早期癌から進行癌に至るまで多くの治療法が適応となり,その組み合わせ,順序を含めると治療の選択肢が多岐にわたる.一方で胃癌,大腸癌,乳癌,肺癌などと違い,症例数が多くないため,大規模な臨床研究を施行することが困難であり,信頼度の高いエビデンスが得られ難い.治療方針を決定するために,特に必要な情報を以下に挙げる.
① 癌の進行度(壁深達度,リンパ節転移,遠隔転移)
② 患者の状態(活動状態,併存疾患,耐術能,臓器能,重複癌)
③ 患者の希望
④ 患者の社会的背景
III.食道癌の診断
食道癌は各種画像診断を用いて腫瘍の壁深達度,リンパ節転移,遠隔転移を評価し,進行度を診断する.病期(Stage)分類は癌の進行程度の客観的記述であり,予後予測や治療選択の根拠,治療成績比較の基準になる.本邦では食道癌取扱い規約第11版2)(2015年4月,日本食道学会編)にしたがって記載する.
1)壁深達度診断
色素内視鏡検査を含む内視鏡検査,NBI観察を含む拡大内視鏡検査,食道造影検査,EUSなどを行い,総合的に診断する.隣接臓器への浸潤診断には,CT・MRI,EUSが有用である.
2)リンパ節転移,遠隔転移診断
頚部・腹部超音波検査,CT・MRI,EUS,FDG-PET,骨シンチグラフィーなどの検査結果から総合的に診断する.
IV.患者の状態の評価
食道癌根治術は消化器癌手術の中で最も侵襲の大きな術式の一つである.外科手術,麻酔,術後管理などの進歩により,食道癌根治術の安全性は高まってきたが,現在においても術後合併症や,在院死亡,手術関連死亡は,他疾患と比較して依然多い.また,食道癌の好発年齢は高齢者層であり,これらの年齢層が併存疾患を有している頻度が高いことに留意する必要がある.したがって,根治手術の適応は,呼吸機能,心機能,肝機能,腎機能,耐糖能等各種重要臓器機能を評価して慎重に決定する必要がある.また,化学療法・放射線療法あるいは化学放射線療法も決して低侵襲でなく,重要臓器の機能が一定の基準を満たしていることが必要である.
食道癌は喫煙・飲酒などの共通のリスクファクターを有する頭頸部癌との重複が多い.他に胃癌,大腸癌,肺癌などが異時性・同時性に重複するため,食道癌診断時に重複癌の検索とその評価を行う必要がある.重複癌を考慮した治療戦略が必要である.
V.食道癌の治療
食道癌の治療方針は上記の食道癌の進行度,患者の状態を評価し,さらに患者の希望や社会的背景を考慮して決定される.食道癌診療ガイドライン(2017年版)では,臨床病期ごとに治療アルゴリズムを作成し,アルゴリズムの分岐点における判断材料に関連したClinical Question(CQ)を抽出し,システマティックレビューが行われている.そして,エビデンスの確実性のみならず,益と害のバランスを重視し,患者側の希望や医療経済的観点も含め検討し,推奨文および推奨度に関して委員の無記名投票を行った上で合意率が掲載されている.なお,無記名投票はガイドライン委員20人のうち,そのCQに対する利益相反のない委員のみで施行された.食道癌診療ガイドラインにおける進行度別のアルゴリズムを示し,進行度別の治療方針を概説する.
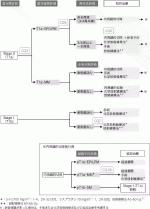
1)cStage0,Ⅰ食道癌治療のアルゴリズム(図1)
cStage0,Ⅰ食道癌の治療方針決定においては,内視鏡検査,頸部・胸部・腹部CT検査,PET検査などによる臨床病期の評価を行う.次に,壁深逹度の評価が,内視鏡切除術(endoscopic resection:ER),手術あるいは化学放射線療法の治療選択に重要である.T1a-EP/LPMとT1a-MMの鑑別においては,超音波内視鏡もしくは拡大内視鏡による精査が弱く推奨されている(CQ3:合意率94.7%[18/19],エビデンスの強さC).壁深逹度の評価に迷う場合,まず侵襲の低いERの適応を考慮する.cStage0(T1a)と診断されERの適応となる場合,ER後狭窄発生のリスクを予測するため病変の周在性評価が必要になる.壁深逹度が内視鏡治療の適応と考えられる食道癌に対しては治療前に周在性の評価を行うことが強く推奨されている(CQ5:合意率100%[20/20],エビデンスの強さA).周在性が3/4周以上の病変の場合は,ER後狭窄のリスクが高いため狭窄予防の処置を講ずる必要がある.狭窄予防としては,予防的バルーン拡張術,ステロイド局注,ステロイド内服のいずれかを行うことが強く推奨されている(CQ6:合意率90%[18/20],エビデンスの強さA).
ER後の組織学的評価は,追加治療の要否を検討する上で極めて重要である.組織学的にpT1a-EP/LPMと診断された場合は経過観察とするが,pT1a-MM/pT1b-SMと診断された場合は追加治療(手術または化学放射線療法)を考慮する必要がある.pT1a-MMかつ脈管侵襲養成である場合,追加治療を行うことが強く推奨されている(CQ18:合意率85%[17/20],エビデンスの強さD).cStageⅠ(T1b)とERにて組織学的にpT1b-SMと診断された場合は,耐術能を評価した上で,外科手術または化学放射線療法の適応を検討する.内視鏡治療の対象とならないcStageⅠ食道癌患者に対して手術を行わない場合,化学放射線療法を行うことが強く推奨されている(CQ7:合意率84.2%[16/19],エビデンスの強さC).
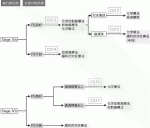
2)cStageⅡ,Ⅲ食道癌治療のアルゴリズム(図2)
cStageⅡ,Ⅲ食道癌の治療方針決定においては,CT検査,上部消化管内視鏡検査,PET検査などによる臨床病期診断を正確に行った上で,まず全身状態の評価により耐術能の有無を判断する.耐術能に問題がない場合には,手術療法を中心とした治療を行うことが弱く推奨されている(CQ8:合意率70%[14/20],エビデンスの強さC).手術療法を中心とした治療を行う場合,術前化学療法と術後化学療法の比較では術前化学療法が強く推奨され(CQ9:合意率89.5%[17/19],エビデンスの強さB),術前化学療法と術前化学放射線療法の比較では術前化学療法が弱く推奨されている(CQ9:合意率100%[18/18],エビデンスの強さC).したがって,第一選択として術前化学療法を施行しその後に根治切除を行う.術前治療を行わない根治切除や術前化学放射線療法も選択肢の一つとなるが,手術を先行した場合は切除標本における病理組織診断に応じて(とくにリンパ節転移陽性例では)術後化学療法を考慮する.術前治療なく手術を行い,病理組織結果でリンパ節転移陽性であった場合には術後化学療法を行うことが弱く推奨されている(CQ11:合意率85%[17/20],エビデンスの強さC).一方で,術前補助療法後に手術を行った場合は,術後化学療法を行わないことが弱く推奨されている(CQ10:合意率85%[17/20],エビデンスの強さD).耐術能はないが化学放射線治療が施行可能な症例や手術拒否例に対しては根治化学法放射線療法(50Gy以上)を考慮し,完全奏効が得られれば以降経過観察を,遺残や再発を来すような場合には救済治療としての外科的切除も検討する.根治化学放射線療法後に完全奏効を得た場合,追加化学療法を行うことが弱く推奨されている術前補助療法後に手術を行った場合は,術後化学療法を行わないことが弱く推奨されている(CQ12:合意率90%[18/20],エビデンスの強さC).なお,耐術能がなく化学放射線療法も適応外の症例に対しては放射線療法(腎機能低下症例,高齢者など),化学療法(放射線照射歴のある患者など)や緩和的対症療法あるいは姑息的な目的での化学療法を考慮する.
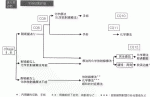
3)cStageⅣ食道癌治療のアルゴリズム(図3)
cStageⅣの治療方針決定においては,他のcStageと同様にCT検査,消化管内視鏡検査,PET検査などによる正確な臨床病期診断に加え,PS(performance status)の評価が重要になる.PS良好な場合はcStageⅣa食道癌において化学放射線療法は根治が期待できる治療選択肢の一つである.cStageⅣa食道癌に対して根治化学放射線療法を行うことは弱く推奨されている(CQ13:合意率85%[17/20],エビデンスの強さC).しかし,化学放射線療法後の遺残に対する救済手術は手術関連死亡が増加する可能性があり,益と害のバランスに十分配慮して総合的に判断する必要がある.cStageⅣa食道癌に対して化学放射線療法後に遺残した場合,手術療法を行わないことが弱く推奨されている(CQ15:合意率85%[17/20],エビデンスの強さD).癌が局所を超えて進行し,全身への治療が必要なcStageⅣb食道癌の場合は化学療法が中心となるが,通過障害がある場合は緩和的放射線療法も考慮される.cStageⅣb食道癌に対して化学療法を行うことは弱く推奨され(CQ16:合意率85%[17/20],エビデンスの強さC),通過障害があるcStageⅣb食道癌に対して緩和的放射線療法を行うことは弱く推奨されている(CQ17:合意率100%[20/20],エビデンスの強さC).一方PS不良な場合は,緩和的対症療法が中心となる.しかしcStageⅣaの場合は放射線治療が食道癌による嚥下障害の改善に有効であり,一定の有害事象を伴うものの長期生存例も得られており,治療選択肢に挙げられる.PS不良なcStageⅣa食道癌に対して放射線療法を行うことは弱く推奨されている(CQ14:合意率95%[18/20],エビデンスの強さD).
VI.おわりに
現在,世界中で多くの多施設共同臨床研究が進行中である.本邦でもcStageⅡ,Ⅲの術前治療に関してはJCOG1109試験が解析中でありその結果が待たれる.手術治療では胸腔鏡下食道切除術が近年急速に普及し,さらにロボット支援下食道切除も保険適用となった.胸腔鏡手術の安全性,根治性,低侵襲性を示すエビデンスレベルの高いデータはなく,JCOG1409試験による検証が待たれる.化学療法では,新たな作用機序を有する免疫チェックポイント阻害薬であるニボルマブの有効性が報告されており3)
4),保険適用となった.バイオマーカーの開発やprecision medicineによる個別化治療による成績の向上が期待され,今後さらなる食道癌診療アルゴリズムのアップデートが期待される.
利益相反:なし
文献
1) 日本食道学会(編):食道癌診療ガイドライン2017年版(第4版).金原出版,東京,2017.
2) 日本食道学会(編):食道癌取扱い規約.第11版,金原出版,東京,2015.
3) Kudo T , Hamamoto Y , Kato K , et al.: Nivolumab treatment for oesophageal squamous cell carcinoma an open-label, multicenter phase 2 trial. Lancet Oncol, 18(5): 631-639, 2017.
4) Kato K , Cho BC , Takahashi M , et al.: Nivolumab versus chemotherapy in patients with advanced oesophageal squamous cell carcinoma refractory or intolerant to previous chemotherapy (ATTRCTION-3):a multicenter, randomized, open-label, phase 3 trial. Lancet Oncol, 20(11): 1506-1517, 2019.
PDFを閲覧するためには Adobe Reader が必要です。