日外会誌. 125(5): 406-414, 2024
特集
乳癌治療における手術の省略について考える
4.早期乳癌ラジオ波焼灼療法の実用化
|
国立病院機構東京医療センター 乳腺外科 木下 貴之 |
ラジオ波焼灼療法(radiofrequency ablation therapy;以下,RFA)などのNSAは正しい適応や手技のもとに実施されれば,従来の外科的切除より高い整容性と劣らない局所制御能があると期待される.本邦では既に肝腫瘍で保険収載されていたRFAが実用化への一番の近道と考え,その適応拡大を試みた.われわれは臨床試験として2006年より臨床使用確認試験および高度医療評価制度下に早期乳癌に対するPhaseⅠおよびⅡの多施設共同臨床試験を実施し,2013年度より先進医療BにてPhase Ⅲ(RAFAELO)試験を開始した.予定登録数は372例で,研究期間は登録期間:60カ月.追跡期間:登録終了後60カ月.総研究期間:120カ月とした.本試験は5年温存乳房内無再発生存割合を主要評価項目とした単アーム試験である.2013年7月に先進医療Bとして承認され,同8月より症例登録が始まり,2017年11月29日に目標登録症例数372例に達し,登録を終了した.そしてRAFAELO試験の安全性と有効性が評価され早期乳癌局所療法として薬事承認・保険収載された.承認条件としてRFAの十分な知識と経験を有する医師が,学会が定めた適正使用指針を遵守し,その使用方法に関する技能や手技に伴う合併症の知識を十分に習得した上で,治療に係る体制が整った医療機関においてRFAが実施されることとされた.
キーワード
ラジオ波焼灼療法, non-surgical ablation therapy (NSA), 保険収載適正使用指針, 早期乳癌
I.はじめに
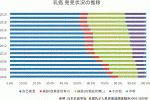
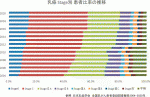
マンモグラフィ検診の普及や画像診断法や針生検の進歩により早期乳癌の発見機会が増加してきている.日本乳癌学会全国乳癌登録では2004年以降,検診が関与した乳癌治療の増加(図1)と乳癌登録数および0期,Ⅰ期の早期乳癌の割合が増加(図2)してきている.乳癌の外科治療では乳房温存療法やセンチネルリンパ節生検に代表される手術の低侵襲化ばかりでなく,高い整容性とQOLへの配慮とも要求されるようになってきた.早期乳癌の乳房温存療法は本邦では1980年代から導入され,その後の長期成績から標準治療としての地位を確立している.最近では,究極の乳房温存療法としてのnon-surgical ablation therapy(以下,NSA)が期待されている.ラジオ波焼灼療法(RFA)は,2006年より臨床使用確認試験および高度医療評価制度下に早期乳癌に対するPhaseⅠおよびⅡの多施設共同臨床試験を実施し,2013年度より先進医療BにてPhase Ⅲ試験を開始し,この試験の結果で早期乳癌RFAの薬事承認および保険収載を目指す方針とした.
II.本邦におけるRFA
RFAは国内では肝臓がんの治療として実績がある.RFA療法の原理は交流電流により電極周囲の組織にイオンの変動が起き,その結果として生じる摩擦熱によりがん細胞を凝固,壊死させるものである.頻用されるCool-tipニードル(17G)での肝臓における焼灼モデルでは,Exposure size 2cmを選択した場合,直径3cmの範囲が焼灼されることになる.この手技を乳癌に応用したもので,当初,肝臓と同じ7本の展開針型ニードルが用いられていたが,乳腺組織が肝臓と比べて硬く穿刺しにくいこと,皮膚への熱伝搬のコントロールが難しいことなどから,現在では,シングルニードルで熱コントロールも容易なCool-tip RF System (Covidien, Energy-Based Devices, Interventional Oncology, Boulder, CO, USA)が主に用いられている.乳癌RFAは,肝臓がん治療ですでに普及している機器を使用するため,機器を有する施設ではニードルの購入のみで実施できるので,わが国では普及する可能性が高い.欠点としては,局所の疼痛が強いため全身麻酔下での実施が推奨されること,局所反応が強いため局所の一過性の浮腫や硬結の残存を認めることなどがあげられる.
乳癌低侵襲治療研究会は,乳癌RFA患者のフォローアップデータやQOLに関する検証の必要があると考え,レトロスペクティブな調査を行い,その結果を高橋らが,2015年San Antonio Breast Cancer Symposiumにて報告した.結果は腫瘍径2cm以下の早期乳癌で,RFAは乳房温存療法と同等の局所成績が確認されたというものであった.
III.海外でのRFA試験
1999年から今日までのRFA後切除試験の報告を表1にまとめた1)
~
13).報告数は多いが,すべてが単施設からの報告で適応やデバイスは異なり完全焼灼率も64~100%である.各々症例数も少数であり機器承認を取得するための十分なエビデンスとなる報告は見当たらなかった.

IV.先進医療Bで実施した早期乳癌RFA多施設共同 Phase III(RAFAELO)試験の概要
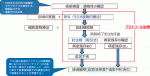
医療技術の概要図を図3に示した.目的は,早期乳癌症例に対して非切除を前提としたRFAを行い,5年温存乳房内無再発生存割合を主要評価項目として乳房部分切除術との同等性を検証し,早期乳癌に対する標準治療の一つとしての位置づけを目指した.対象は,Tis-T1(腫瘍径1.5cm以下)N0M0,Stage 0-Ⅰの単発乳癌病変を有し,術後の化学療法,放射線療法,ホルモン療法に耐えうる症例.また,重篤な脳梗塞,心筋梗塞,血栓塞栓症の既往歴がなく,全身麻酔に耐えうることとした.術前診断はマンモグラフィ・超音波検査に加えて造影MRI検査を必須とし,細胞診でなく針生検で確定診断することとした.治療は,全身麻酔下で,体表面から乳房内病変に対して超音波ガイド下にラジオ波電極針を穿刺し,病変にラジオ波による熱焼灼を行う.予定登録数は372例で,研究期間は登録期間:60カ月.追跡期間:登録終了後60カ月.総研究期間:120カ月である.本試験は5年温存乳房内無再発生存割合を主要評価項目とした単アーム試験である.本試験の概要を図4に示した.2013年7月に先進医療Bとして承認され,同8月より症例登録が始まった.研究参加施設は,これまでの実績より北海道がんセンター,群馬県立がんセンター,千葉県がんセンター,国立がん研究センター中央病院,国立がん研究センター東病院,岐阜大学医学部附属病院,岡山大学医学部附属病院,広島市立広島市民病院,四国がんセンターの9施設とした.2016年1月10日にプロトコールで予定されていた中間解析が実施され,効果安全性評価委員会にて試験継続が承認された.その後も症例登録は順調に進み2017年11月29日に目標登録症例数372例に達し,登録を終了した.
本医療技術は2021年1月に日本乳癌学会から厚生労働省医療ニーズの高い医療機器の早期導入に関する検討会(医療ニーズ検)に早期導入の要望書が提出された.2021年11月開催されたニーズ検討会にて「早期導入品目」に選定されたため,PMDAへ提出する短期解析報告書を作成し,早期に薬事承認と保険収載を目指す準備をはじめた.
2023年7月7日にRAFAELO試験の短期成績が信頼性,有効性および安全性の点で評価され,RFAの早期乳癌に対する適応拡大の薬事承認を取得した.Cool-tipTM RFAシステムEシリーズの使用目的または効果に「乳腺腫瘍(腫瘍径1.5㎝以下の単発,触診および画像診断による腋窩リンパ節転移および遠隔転移を認めない限局性早期乳癌)に対する治療を目的とした凝固および焼灼.」が追加された.
承認条件を1.ラジオ波焼灼システムによる治療に関連する十分な知識および経験を有する医師が本品の使用方法に関する技能や手技に伴う合併症等の知識を十分に習得した上で,治療に係る体制が整った医療機関において本品を用いるよう,関連学会との協力により作成された適正使用指針の周知,講習の実施等,必要な措置を講ずること.とされた.
その後,2023年12月1日に本品の早期乳癌への使用が保険収載された.


V.適正使用指針
薬事承認の際に,乳癌RFAの承認条件として日本乳癌学会に適正使用指針の作成と会員への周知が示された.日本乳癌学会では,施設要件(表2),術者要件(表3),患者選択基準(表4),標準的治療法(表5)と標準的実施手順を作成し会員および市民へ公開した.また,RFA術者認定の条件を,①施設要件および術者要件を満たすこと,②eラーニング受講(術者用と病理医用)③NCD乳癌登録に実装したRFA症例登録システムへ症例登録すること(3年間目途)とし,術者申請内容を学会認定委員会にて審査することとした.




VI.標準的なRFA実施手順
RFAの標準的実施手順は早期乳癌へのRFAを「体表面から乳房内病変に対して画像ガイド下にラジオ波電極針を穿刺し,病変にラジオ波による焼灼を行う手技」と定義する.
以下に実際の手順を示す.
1)麻酔:全身麻酔にて,手術室で行うこととする.
2)使用器材:COVIDIEN社 Cool-tipTM RFAシステムEシリーズ.
3)焼灼時間:タイマー設定は30分に設定するが,特に制限は設けない.
4)穿刺方法:可及的に腫瘍の最大割面に対し平行となるよう,また腫瘍の中心を通るように穿刺する.穿刺部位はこだわらないが,穿刺部位(皮膚)の熱傷を避ける.
5)出力方法:5Wから出力を開始し,1分経過時に10Wに設定,それ以降は1分毎に5または10Wずつ出力を上げていく.出力の上限値は設けず,出力に限界がある場合は,その出力にて焼灼を継続する.
6)焼灼範囲:腫瘍縁から1cmのマージンを目標とし,ニードルポジションを設定する.焼灼中の超音波画像にて腫瘍の不明瞭化とマイクロバブルの範囲を確認し,十分な焼灼エリアを確保する.
7)熱傷予防:皮膚熱傷,胸壁熱傷を予防するために,皮下組織内に適宜5%ブドウ糖液の注入を行う.また,通電中は氷嚢にて皮膚冷却を行い,必要に応じて術後も冷却を継続する.
8)焼灼判定:焼灼度合いが増してくると,電気抵抗値が上昇してくる.一定値以上,抵抗値が上昇するとシステムは出力を中断する.この現象をロールオフ(もしくはブレイク)と称する.1回目のロールオフ後にポンプを停止し,ニードルの焼灼温度を測定する.焼灼温度が70度以下の場合は,焼灼不良とし同じ場所にて焼灼を追加する.複数回の追加焼灼をもってしても70度に達しない場合は,焼灼終了時の画像所見を参考に治療を中止するか否かを判断する.
9)センチネルリンパ節生検を実施する場合は,原則的にRFA開始前に行うこととする.
10)術後は学会が定めた治療プロトコール(図5)に従い経過観察を行う.
Ⅶ.おわりに
乳癌の究極の低侵襲局所療法であるRFAなどのNSAは正しい適応や手技のもとに実施されれば,従来の外科的切除と比較して同等の治療成績であることが確認された.本邦では既に他疾患で保険収載されているRFAが実用化への一番の近道と考え,その適応拡大を試みた.厚生労働省医療ニーズの高い医療機器の早期導入に関する検討会(医療ニーズ検)での審議を経て,RAFAELO試験の安全性と有効性が評価され早期乳癌局所療法の選択肢の一つとして薬事承認,保険収載された.RFAの十分な知識と経験を有する医師が,その使用方法に関する技能や手技に伴う合併症の知識を十分に習得した上で,治療に係る体制が整った医療機関においてRFAが実施されることが承認条件とされた.
利益相反:なし
文献
1) Jeffrey SS , Birdwell RL , Ikeda DM , et al.: Radiofrequency ablation of breast cancer. Arch Surg, 134: 1064-1068, 1999.
2) Izzo F , Thomas R , Delrio P , et al.: Radiofrequency ablation in patients with primary breast carcinoma. Cancer, 92: 2036-2044, 2001.
3) Burak WE Jr , Agnese DM , Povoski SP , et al.: Radiofrequency ablation of invasive breast carcinoma followed by delayed surgical resection. Cancer, 98: 1369-1376, 2003.
4) Singletary SE . Feasibility of radiofrequency ablation for primary breast cancer. Breast Cancer, 10: 4-9, 2003.
5) Hayashi AH , Silver SF , van der Westhuizen NG , et al.:Treatment of invasive breast carcinoma with ultrasound-guided radiofrequency ablation. Am J Surg, 185: 429-435, 2003.
6) Fornage BD , Sneige N , Ross MI , et al.: Small breast cancer treated with US-guided radiofrequency ablation:feasibility study. Radiology, 231: 215-224, 2004.
7) Noguchi M , Earashi M , Fujii H , et al.: Radiofrequency ablation of small breast cancer followed by surgical resection. J Surg Oncol, 93: 120-128, 2006.
8) Khatri VP , McGahan JP , Ramsamooj R , et al.: A phase Ⅱ trial ogf image-guided radiofrequency ablation of small invasive breast carcinoma:use of saline-cooled tip electrode. Ann Surg Oncol, 14: 1644-1652, 2007.
9) Medina-Franco H , Soto-Germes S , Ulloa-Gómez JL , et al.: Radiofrequency ablation of invasive breast carcinoma:A phase Ⅱ trial. Ann Surg Oncol, 15: 1689-1695, 2008.
10) Garbay JR , Mathieu MC , Lamuraglia M , et al.: Radiofrequency thermal ablation of breast cancer local recurrence:A phase Ⅱ clinical trial. Ann Surg Oncol, 15: 3222-3226, 2008.
11) Imoto S , Wada N , Sakemura N , et al.: Feasibility study on radiofrequency ablation followed by partial mastectomy fot stageⅠ breast cancer patients. Breast, 18: 130-134, 2009.
12) Kinoshita T , Iwamoto E , Tsuda H , et al.: Radiofrequency ablation sa local therapy for early breast carcinomas. Breast Cancer, 18: 10-17, 2011.
13) Ohtani S , Kochi M , Ito M , et al.: Radiofrequency ablation of early breast cancer followed by delayed surgical resection. – a promising alternative to breast-conserving therapy. Breast, 20(5): 431-436, 2011.
PDFを閲覧するためには Adobe Reader が必要です。