日外会誌. 125(3): 252-257, 2024
会員のための企画
わが国におけるがんゲノム医療の現在と未来―パネル検査から全ゲノム解析研究を含めて―
|
1) がん研究会有明病院ゲノム診療部,乳腺センター乳腺内科,国立高度専門医療研究センター医療研究連携推進本部全ゲノム解析等事業実施準備室臨床・患者還元支援チームマネージャー 深田 一平1) , 上野 貴之2) |
近年,「がん細胞」に起きている遺伝子の変化を調べ,その特徴を知ることで,個々のがんの病態把握や病状に適した,より効果的・効率的ながん治療を行うことが期待されている.2018年3月に閣議決定された第3期のがん対策推進基本計画において「がんゲノム医療」の文言が盛り込まれ,がんゲノム医療の推進に向けて必要な体制整備等を進められ国民皆保険制度の下で本格的な運用が始まった.さらに,2019年12月末公表された全ゲノム解析等実行計画(第1版)のもと,全ゲノム解析等を進めることにより,一人ひとりにおける治療精度を格段に向上させ,治療法のない患者に新たな治療を提供するといったがん医療の発展や,蓄積されたデータを研究・創薬などへ活用,ひいては,がんの克服を目指した取組みが国を挙げて推進されている.このような状況の中,全ゲノム解析等の事業化に向けて2023年4月に事業実施準備室が発足している.わが国において実践が進んでいるがん遺伝子パネル検査を用いたがんゲノム医療の現状について解説するとともに,全ゲノム解析等実行計画における全ゲノム解析結果の患者還元に関する取組みを紹介しながら,わが国における,がん全ゲノム解析の現状とその将来展望について紹介する.
キーワード
がんゲノム医療, 個別化医療, 遺伝子パネル検査, 全ゲノム解析
I.はじめに
近年,「がん細胞」に起きている遺伝子の変化を調べ,その特徴を知ることで,個々のがんの病態把握や病状に適した,より効果的・効率的ながん治療を行うことが期待されている.わが国においてはがんゲノム医療の推進に向けた医療提供体制の整備が進められ,2019年6月にがん遺伝子パネル検査が保険収載されたことにより国民皆保険制度の下で実践が進んでいる.さらに,2019年12月末に厚生労働省から全ゲノム解析等実行計画(第1版)が公表され,全ゲノム解析等を進めることにより,一人ひとりにおける治療精度を格段に向上させ,治療法のない患者に新たな治療を提供するといったがん医療の発展や個別化医療の推進など,がんの克服を目指したがん患者のより良い医療を届けるための取組みが政策として推進されている.本稿では,がんの発生や薬剤耐性等に関わる複数のがん関連遺伝子について,次世代シークエンサーを用いて一度に調べる「がん遺伝子パネル検査」を用いたがんゲノム医療の現在と,国を挙げて取組みが進められている,がん全ゲノム解析の概要について解説する.
II.がんゲノム医療提供体制の整備
米国では2015年1月の一般教書演説において,オバマ大統領(当時)が“Precision Medicine Initiative”を発表し,さらに2016年1月にはバイデン副大統領(当時)の主導で,がんの新しい診断法や治療法を開発しがんの克服を目指す“Cancer Moonshot”プロジェクトが立ち上げられるなど,国家プロジェクトとしてゲノム研究や医療の取組みが推進されている.英国では,英国保健省によって2013年に設立されたGenomics Englandが,主に,がんおよび稀少疾患を対象に,患者等の全ゲノム解析を行う“100,000 Genomes Project”を実施しており,2018年12月,10万ゲノム解析の終了を公表した.
わが国においては,第3期がん対策推進基本計画に基づいた,がんゲノム医療提供体制の整備が進められ,2023年12月現在,厚生労働省が指定した,がんゲノム医療を牽引する高度な機能を有する医療機関である「がんゲノム医療中核拠点病院」(13箇所)や「がんゲノム医療拠点病院」(32箇所),これらと連携してがんゲノム医療の提供を行う「がんゲノム医療連携病院」(214箇所)で,がん遺伝子パネル検査を実施することが可能となっている.また,2018年6月には,がんゲノム医療中核拠点病院等からゲノム情報や臨床情報を集約,管理,利活用等を行う「がんゲノム情報管理センター(Center for Cancer Genomics and Advanced Therapeutics:C-CAT)」が設置され,解析したゲノム情報等を参考に最新の医学的知見に基づく診療を行うと同時に,新たな医薬品等の開発にも利活用する体制の構築を進めている(図1).
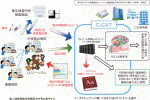
III.保険診療における遺伝子パネル検査の流れ
遺伝子パネル検査は,次世代シークエンサー等を用い,がんに関連する多数の遺伝子を一度に解析することで,治療方針の決定を補助し,がんの治療成績の向上につながることが期待されている.
2019年6月に「がん遺伝子パネル検査」が保険適用となり,2023年12月現在,5種類(OncoGuideTM NCCオンコパネルシステム,FoundationOneⓇ CDx がんゲノムプロファイル,FoundationOneⓇ リキッドCDx がんゲノムプロファイル,Guardant360 CDx がん遺伝子パネル,GenMineTOPがんゲノムプロファイリングシステム)の遺伝子パネル検査を用いて国民皆保険制度の下で本格的に運用されている.保険適用された遺伝子パネル検査は,「次世代シークエンサー等を用いた遺伝子パネル検査に基づくがん診療ガイダンス」に従い,標準治療のない固形がん患者,もしくは標準治療が終了となった固形がん患者(終了が見込まれる者を含む)が対象となっている.現在,保険診療として実施可能な遺伝子パネル検査の概要を示す(表1).
遺伝子パネル検査は,がんゲノム医療中核拠点病院,がんゲノム医療拠点病院,およびがんゲノム医療連携病院で実施される.検査の流れとしては,まず,担当医等による遺伝子パネル検査実施の医学的な必要性や妥当性が検討された上で,患者に対し十分なインフォームド・コンセントを行った後,がんの病理組織等の検体が準備され,次世代シーケンサー等による多遺伝子の変異解析が行われる(検体提出時44,000点).解析結果により得られた検査結果は,多職種(がん薬物療法に関する専門的な知識および技能を有する医師,遺伝医学に関する専門的な知識および技能を有する医師,遺伝カウンセリング技術を有する者等)による検討会(エキスパートパネル)で,その結果の医学的解釈について議論された上で患者に返却・説明(結果説明時12,000点)される.なお,エキスパートパネルにおいては,主治医による治療決定の補助を目的として,検査会社から返却された結果と,C-CATが作成した当該患者に係る調査結果(患者がC-CATへのデータ提出について同意した場合)を用いて,治療効果が期待される医薬品の選択,予後予測,2次的所見の取り扱い等について議論が行われる.

IV.遺伝子パネル検査を用いた治療
本邦における標準治療後の患者における治療薬へのアクセスに関して,遺伝子パネル検査を用いた先行研究では,遺伝子解析を行うことができた患者のうち,約半数でアクショナブル遺伝子の異常が発見され,25例(13.4%)の患者で個々の遺伝子異常に合った治療薬の投与が可能であった1).パネル検査の結果,判明した遺伝子変異等に基づいたエキスパートパネルでの検討を経て,主治医により,治験薬や適応外使用薬の投与が検討されるが,保険診療における遺伝子パネル検査の現状としては,2019年6月~2022年6月末までにC-CATに登録された30,822件の遺伝子パネル検査において,その結果が治療に結びついた割合が9.4%(2,888例)と報告されている2).わが国においては,上記のように,標準治療後の患者に対して遺伝子変異に対応した治療薬が届けられるのは,パネル検査を受けた患者の10%程度であり,パネル検査後の治療到達率を向上させる取組みが重要である.
V.全ゲノム解析等実行計画(第1版)の公表
2019年12月に全ゲノム解析等実行計画(第1版)が厚生労働省より公表された3).その中で,一人ひとりの治療精度を格段に向上させ,治療法のない患者に新たな治療を提供するといったがんや難病等の医療の発展や,個別化医療の推進等,がんや難病等患者のより良い医療の推進のために全ゲノム解析等を実施することが明記され,国を挙げて,全ゲノム解析,患者還元,解析・データセンター,データ利活用,検体保存・利活用,事業実施組織の検討が進められている.
VI.令和3年度AMED研究班の概要(がん領域)
令和3年度革新的がん医療実用化研究事業において,がんの本態解明に関する研究として,がん全ゲノム情報の活用によるがん個別化医療の確立に関する研究が開始された.本研究は下記の三つの分野に大別される(表2).
A班)患者還元班(体制構築班):がん全ゲノム解析等における患者還元に関する研究
がん患者の臨床解析を行い,レポート作成およびエキスパートパネルによる協議等をへて患者還元を行う(新規の患者および検体保存済みの患者).
B班)領域班:難治性がん(食道がん等の消化器がん、白血病等の血液がん、小児がん、希少がん、卵巣がん等の婦人科がん、呼吸器がんや乳がん等の6領域)の全ゲノム配列データおよび臨床情報等の収集と解析に関する研究
領域別のがん患者について,C班と連携して全ゲノム解析等を行い,患者還元を行う(検体保存済みの患者).
C班)解析班:がん全ゲノム解析等におけるゲノム解析・臨床応用に関する研究
A,B班において解析対象になったがん患者について,臨床情報を収集するとともに統一パイプラインによる解析および臨床解析を行う.また,解析・データセンターの構築に向け高度な横断的解析,データ共有システムの構築等にも取り組む.
【AMED研究班における全ゲノム解析等の研究成果(がん領域)】
① これまでの全ゲノム解析等の出検数
2023年5年11月20日時点において,がん領域12,446例,難病領域8,033の計20,479例の全ゲノムデータが格納されている.
②患者還元班(A班)における研究成果
1)患者還元班のこれまでの成果
2023年度2月20日時点で,全ゲノム解析等の結果に基づくエキスパートパネルが1,163例実施され,治療薬の選択や診断,遺伝性疾患の診断に有用なアクショナブル変異を641例に検出した.その中で,
・既存の検査では検出できないがんに関与するゲノム異常の検出:143例
・全ゲノム解析の結果が診断に有用であった症例:51例
・がん以外の疾患に関与する可能性が高いゲノム異常を検出:52例
であったことが報告されている.
2)WGSが診断に有用であった解析結果の1例(図2)
がん研有明病院(上野班)の解析結果の1例を紹介する.耳下腺腫瘍(acinic cell carcinoma)の症例において,全ゲノム解析による構造変異解析を行ったところ,腺房細胞癌(acinic cell carcinoma)において生じることが報告されている4番染色体と9番染色体の転座[t(4;9)(q13;q31)]が検出された.この構造変異により,4q13に存在する唾液腺に特異的な発現を示す遺伝子群SCPP(The secretory Ca-binding phosphoprotein) clusterのエンハンサーが9q31に存在するNR4A3に近接し,その発現を上昇させることが知られており,また,NR4A3は転写因子であり,下流のCCND1発現の活性化などを通じて細胞の増殖に寄与すると考えられている.
このような「エンハンサーが本来転写を活性化する遺伝子とは異なる遺伝子に作用する」現象 “Enhancer hijacking” を伴う構造変異は,融合遺伝子を生じる構造変異とは異なりRNA-Seqで検出することができず,全ゲノムシークエンシング解析を行うことで初めて可能となった解析であると言える.


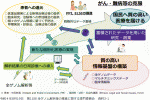
VII.おわりに
保険診療において実装が進められている遺伝子パネル検査によるがんゲノム医療の充実を図るとともに,より質の高い医療を国民に届け,将来的な「がん・難病等の克服」をするために,創薬等を見据えた出口戦略に基づく新規の臨床試験・治験等による経時的で質の高い臨床情報と全ゲノム情報に加えて,マルチオミックスデータや,リアルワールドエビデンスが集積された情報基盤構築といった戦略的なデータの蓄積を進め,それらを用いた研究・創薬などを促進することが重要である.また,全ゲノム解析解析結果の日常診療への早期導入や,新たな個別化医療の実現についても推進することが期待されている(図3).
利益相反:なし
文献
1) Sunami K , Ichikawa H , Kubo T , et al.: Feasibility and utility of a panel testing for 114 cancer-associated genes in a clinical setting: A hospital-based study. Cancer Sci, 110(4): 1480-1490, 2019.
2) 国立がん研究センターがんゲノム情報管理センター:C-CAT登録状況.2023年12月24日. https://for-patients.c-cat.ncc.go.jp/registration_status/
3) 厚生労働省ホームページ:全ゲノム解析等実行計画について.2023年12月24日. https://www.mhlw.go.jp/stf/newpage_08564.html
PDFを閲覧するためには Adobe Reader が必要です。