日外会誌. 124(4): 336-341, 2023
特集
外科的冠動脈血行再建術の現状と展望
5.MICS CABG
|
兵庫医科大学 心臓血管外科 坂口 太一 |
近年冠動脈治療におけるハートチームの重要性が強調されるようになり,冠動脈バイパス術(CABG:coronary artery bypass grafting)と経皮的冠動脈インターベンション(PCI:percutaneous coronary intervention)の特性を考慮しながら,個々の患者に合わせた冠動脈血行再建法を選択することが推奨されている.そのような状況において低侵襲冠動脈バイパス術(MICS CABG:minimally invasive CABG)は正中切開によるCABGとPCIの間に位置するものとして注目を集めている.最近では両側内胸動脈(BITA:bilateral internal thoracic arteries)を用いたMICS CABGやロボットによる完全内視鏡下多枝CABG(TECAB:totally endoscopic coronary artery bypass)の良好な成績も報告されている.長期成績についてはさらなる検証が必要であるが,低侵襲化の流れのなかで,PCIとのハイブリッド治療を含めた包括的な冠動脈血行再建の選択肢の一つとして,MICS CABGは今後ますます注目されると考えられる.
キーワード
低侵襲心臓手術, 冠動脈バイパス術, オフポンプ, MICS
I.はじめに
肋間小開胸による低侵襲心臓手術(MICS:Minimally Invasive Cardiac Surgery) は,弁膜症手術を中心に広く普及しているが,近年CABGに対するMICSが注目されている.従来の左前下行枝(LAD:left anterior descending artery) 一枝病変に対するMIDCAB(Minimally invasive direct coronary artery bypass)に加え,多枝病変に対するMICS CABGが一部の施設で行われるようになり,PCIとのハイブリッド治療などを組み合わせることにより,その適応が広がりつつある.
II.MICS CABGの変遷
主として左内胸動脈(LITA:left internal thoracic artery)とLADの一枝バイパスを行うMIDCABが1996年にCalafioreらによって発表され1),翌年にはOPCAB(off-pump coronary artery bypass)とともにわが国に導入され,拡がりをみせた.しかし当時のデバイスではLITAの十分な剥離や多枝バイパスが困難なことなどから,1998年をピークにその手術数は減少し,正中切開による多枝OPCABが主流となった.ところが,MICS関連デバイスの発展にともない,左小開胸による多枝MICS-CABGの臨床成績がMcGinnらによって報告された2009年頃から,MICS CABGが再び注目されるようになった2).開胸部位をより外側にすることでLITAの全長剥離が容易になり,特殊なスタビライザーとハートポジショナーによって全ての部位にオフポンプによるバイパスが可能になった.ロボットによってITAを採取し,LITA-LAD吻合を小開胸直視下に行うrobot-assisted MICS CABGも同時期より一部の施設で開始されるようになった.
2014年のヨーロッパのガイドラインでは,LAD一枝病変に対するMICS CABGがclass Ⅱaとしてガイドラインにも記載されるようになり,MICS CABGの適応が拡がりつつある.
III.MICS CABGの方法
MICS CABGを左肋間開胸によるCABGと定義するなら,現在MICS CABGは次のような方法で行われている.
1)直視下によるMICS CABG(off-pumpまたはon-pump)
McGinnらは従来のMIDCABより外側で開胸し,経胸壁的に挿入したスタビライザーとポジショナーによって胸腔内での心臓の脱転を行い,全ての冠動脈領域にオフポンプによるバイパスが可能なことを2009年に発表し,MICS CABGと名付けた.上行大動脈をサイドクランプして大伏在静脈(SVG:saphenous vein graft)の中枢吻合を行い,LAD以外の冠動脈に吻合するもので,多枝MICS CABGが普及するきっかけとなった.彼らは連続450例の検討を行い,(平均年齢62.3±10.7歳,平均バイパス本数2.1±0.7本),手術死亡率1.3%,胸骨正中切開への移行3.8%,再開胸率2.2%と報告している2).さらにMICS CABGと正中切開OPCABの比較において,MICS-CABGは創感染が少なく,術後回復が良好であったと報告している3).オタワ大学のグループは連続510例のMICS CABGの長期成績を検討し,30日以内死亡0.2%,MACCE発生率1.4%,10年生存率90.3%,MACCE回避率87.1%と良好な成績を報告している4).グラフト開存率に関しては,同グループより6カ月の開存率が92%(LITAは100%)と良好な成績が報告されている5).
KikuchiらはMcGinnらの方法を応用し,左小開胸から直視下にBITAを採取し,in-situ graftとして使用しうることを2015年に報告した6).この方法により全動脈グラフトによる完全血行再建が可能で,さらに上行大動脈に操作を加えないため脳梗塞のリスク軽減が期待される.Harmonic scarpelを用いたskeletonize法によって十分な長さのRITAを採取が可能で,72%の症例でin-situ graftとしてRITAを使用している7).直視下のBITA採取はいくつか報告されているが,多くはRITAをfree graftにしてLITAの側枝に吻合し,Y-composite graftとして用いたり,RITAをRAやSVGで延長してI-composite graftとして使用するものである.NambiarらはBITAを直視下に採取しLITA-RITA Yグラフトとして用いたMICS-CABG 819例の手術死亡率0.7%,正中移行率 0.4%,出血再開胸 0.6%,1年後のグラフト開存率99.5%と良好な成績を報告している8).
2)直視下によるMICS CABG(心停止下)
Babliakらは左前胸部切開下にon-pump arrested heartによる多枝MICS CABGを行っている.第2肋間から挿入したChitwoodクランプを用いて上行大動脈を遮断し心停止を得たあと,下大静脈と左上下肺静脈を別々にテーピングし牽引することで,すべての冠動脈領域に吻合することが可能である.連続170例の報告では,平均3.1±0.7本のバイパスを行い,大動脈遮断時間は71±19分,体外循環時間135±26分,総手術時間258±43分で,周術期死亡や心筋梗塞は認めなかった9).胸骨切開はしないものの人工心肺下心停止にて行うこの方法がMICSと呼ぶべきか議論はあるものの,技術的なハードルが低くヨーロッパを中心に実施施設が増えているようである.
3)Robot-assisted MIDCAB(RA-MIDCAB)
Davinciを用いたロボット支援下MICS CABGとして最も一般的なもので,ロボット下にLITAを採取し,LADとの吻合を直視下に行うものである.第一世代のDaVinciが導入された1990年代後半から一部の施設で継続的に行われており,Giambrunoらは1998年から2016年までに単一施設で行われた605例の手術死亡率が0.3%,LITA-LADの開存率が97.4%と良好な成績を報告している10).
4)Totally endoscopic CAB(TECAB)
ITA採取だけでなく冠動脈吻合もロボットで行うもので,肋間開胸は行わず,8〜12mmのポートのみで手術が完結する.体外循環を使用する施設が多いなかBalkhyらは544例のoff-pump TECABを行い,その中期成績を報告している.約半数でBITAをin-situあるいはY-composite graftとして使用している.前半は末梢吻合デバイスを用いていたが,後半は通常のCABGと同様に手縫いによる連続縫合を行っている.これらの操作はすべてロボットによる完全内視鏡にて施行しており,正中コンバージョン1例,手術死亡率0.9%,早期グラフト開存率97%,38カ月のMACE回避率92.5%と成績は良好であった11).
IV.MICS-CABGのラーニングカーブ
Uneらは210例の連続MICS-CABGのラーニングカーブについて検討している12).それによれば,初期のオフポンプ多枝MICS-CABG症例で胸骨正中切開への移行を10例(14.5%)に認めたが,手術死亡はなく,経験値の上昇と手術成績に関連はみられなかった.しかしオフポンプ多枝MICS-CABGの手術時間は,経験症例数と有意に負の相関を示し,CUSUM解析を行うとその手術時間は17例目でunacceptableを脱し,44例目でacceptableとなった.一方,オンポンプ MICS-CABGでは相関は認めず,初期の症例でも手術時間はacceptableであった.このことから,多枝MICS-CABGを導入する際には,オンポンプCABGから開始することを推奨している.
Robotic-assisted MIDCABのラーニングカーブに関してGiambrunoらは,初期の200例では正中切開へのコンバージョンが16%あり,後半405例では6.9%に減少したと報告している10).STSデータベースを用いた2014年から2019年に行われた1,195例の解析では,ラーニングカーブ曲線は急峻で,10例を境に正中コンバージョン率は7.7%から2.5%,再開胸率は18.9%から10.8%,主要合併症率は21.7%から12.9%と減少したものの,手技成功率は72.9%から85.4%の上昇と満足し得るものではなかった13).Giambrunoらの報告とは時代背景が違うが,Robotic-assisted MIDCABのラーニングカーブの問題は依然看過できないようである.
V.PCIとのハイブリッド治療
近年冠動脈血行再建におけるハートチームの役割が重要視されるとともに,MIDCABとPCIとのハイブリッド治療(HCR:Hybrid Coronary Revascularization)が最注目されている.HCRとconventional CABGを比較したメタアナリシスによれば,HCRの周術期合併症発生率はCABGと同等あるいは低く,特に輸血率が少なく術後回復が早いなどの利点がある一方,再血行再建率が高いとされている14).一方,HCR,CABGおよびPCI のpropensity score-matching studyでは,再冠血行再建を含む心脳血管有害事象(MACCE)発生率においてHCRはPCIより低く,CABGと同等であった.さらにEuroSCORE高値のハイリスク群において,HCRはCABGやPCIよりもMACCE発生率が有意に低く,SYNTAX score高値の複雑病変症例において,HCRのMACCE発生率はCABGと同様でPCIより有意に低かった15).このことはHCRが侵襲性においてCABGより,血行再建においてPCIより優れていることを示しており,PCIの低侵襲性とCABGの虚血改善効果の両者を兼ね備える治療として一定の患者に有用であることを示している.HCRとCABGを比較した唯一の前向き無作為試験であるHYBRID trialでは,術後5年における全死亡率,MACCE発生率は両治療間で有意差を認めなかった16).
多枝MICS CABGとPCIのHCRはその恩恵をさらに拡大しうるものとして注目されている.特にBITAを用いたaortic no-touch MICS CABGとのHCRは冠動脈疾患に対する低侵襲治療の一つの完成形かもしれない.BalkhyらはロボットによるBITAを用いたTECABとPCIのハイブリッド治療156例の中期遠隔成績を報告している.それによると平均在院期間は2.7日,正中コンバージョンや脳梗塞,心筋梗塞などは認めず,早期グラフト開存率は98%と短期成績は良好であった.さらに8年における心臓関連死亡率3.9%,MACCE回避率94%と遠隔成績も良好であった17).HCRは高齢者やフレイルな患者が一般的に良い適応とされているが,BITAを用いることにより若年者においてもその適応が広がる可能性があり,今後の発展が期待される.
VI.MICS CABGの実際
われわれは2013年12月にMICS CABGを導入し,これまで210例に施行してきた.当初はMcGinnらと同様,直視下にLITAを採取してLADに吻合し,上行大動脈を部分遮断して大伏在静脈や橈骨動脈の中枢吻合を行っていたが,BITAの採取を開始してからは,上行大動脈に操作を加えずにin-situ BITAまたはITAとのコンポジットグラフトを用いて多枝バイパスを行っている.
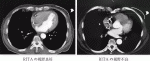
MICS CABGの適応を決めるため可能な限り心臓CTを施行するようにしている.左肺の高度癒着が疑われる症例,LADが明らかに心筋内走行をしている症例は適応外としている.多枝MICS CABG症例では,大腿動脈送血によるon-pump CABGへの術中移行も考慮し,大動脈の性状が不良で逆行性送血のリスクの高い症例は適応から外すことが多い.BITA採取例では,漏斗胸のように胸骨背面がRITAより背側にあるような症例は適応外としている(図1).三次元構築画像を検討して開胸肋間を決定するが,ほとんどが第5肋間開胸としている.
左右分離換気とし,CTで術前計測したLADの予想部位より外側に約8cmの皮膚切開をおく.多枝バイパス症例ではそれよりも2cm程度外側を切開する.ケント鉤などを用いてThoraTrack® MICS開胸器の頭側bladeを上方に牽引し,LITAの視野を確保する.その際ブレードの先端がLITAに接触していないことを必ず確認する.RITAを採取する際はOctopus Nuvo®スタビライザーなどを用いて右肺を右下方に圧排して視野を確保する.
Composite graftを作成する時は,第1または第2肋間の小切開孔からITAを体外に誘導して吻合操作を行う.LITAとのY-composite graftは胸腔内でも作成可能であるが,体外で作成するほうがLITAの近位部に正確に吻合することができるため,吻合部出血や解離などのトラブルを予防できると考えている.
次に心膜を切開するが,多枝バイパス症例では心尖部から大動脈遠位翻転部付近まで切開する.側壁や後壁に末梢吻合を行う場合は,さらに横隔膜面に沿って下大静脈付近まで心膜を切開すると,心臓の脱転が容易になる.麻酔はややドライ管理とし,胸腔内における心臓の脱転の妨げにならないよう留意する.
末梢吻合においては,前下行枝,対角枝などは標的冠動脈の展開が容易であるが,側壁,後壁の冠動脈に吻合する際は,複数のdeep pericardial sutureをおいて吻合部位を徐々に展開していくとよい.armless Starfish18)やTentacles NEO19)のような種々のポジショナーは狭いworking spaceでの視野展開に有用である.それでも視野確保が困難なときは,体外循環補助下の吻合を考慮する.閉鎖回路を用いた部分体外循環のみで,視野確保は容易になる.
吻合終了後,心尖部付近の心膜は閉鎖するが,前下行枝吻合部より頭側は開放して,グラフトを圧迫しないようにする.心膜の脂肪組織を寄せてLITAをカバーし,肺の癒着を予防する.
VII.MICS CABGの経験
2013年12月から2022年12月まで単独術者においてMICS CABGを予定した215例のうち,MICSを完遂したのは210例であった.正中切開コンバージョンとなった5例の内訳を表1に示す.いずれも前半に起こっており,術前造影CTを丁寧に検討すれば回避できたものと考えている.平均年齢は73±11歳(38〜89歳),グラフト本数は1枝100例,2枝76例,3枝28例,4枝4例であった.多枝バイパス110例のうち半数の55例にBITAを使用した.体外循環は主として導入初期の25例に使用した.同時手術として経カテーテル大動脈弁留置術(TAVI:transcatether aortic valve implantation)を6例(経心尖3例, 経大腿3例),左室瘤切除術と左心耳切除術をそれぞれ2例に施行した.PCIとのHCRを33例に行った.手術死亡は3例(癌,透析患者の非閉塞性腸管虚血)で,合併症としては出血再開胸1例(透析患者の再々手術例),遅発性タンポナーデ1例(透析症例),脳梗塞1例(経心尖TAVI併施症例),抜管遅延4例などであった.早期グラフト開存率は97.8%(351/359)であった.前期122例の5年におけるMACCE回避率は91.7%であった20).

VIII.おわりに
ISCHEMIA trialでは安定狭心症に対して一律に早期血行再建を行うことが,必ずしも患者にとって有益ではないことが示唆された.いいかえれば,画一的に治療を行うのではなく,一人一人の患者の状況に合わせて治療方針を決める重要性を再認識させるものとなった.そういった状況のなかでHCRを含めたMICS CABGは,多枝冠動脈病変に対する治療選択肢を広げるものとして,今後普及していくと考えている.
利益相反
講演料など:日本メドトロニック株式会社
文献
1) Calafiore AM, Di Giammarco G, Teodori G, et al.: Left anterior descending coronary artery grafting via left anterior small thoracotomy without cardiopulmonary bypass. Ann Thorac Surg, 61: 1658–1665, 1996.
2) McGinn JT Jr, Usman S, Lapierre H, et al.: Minimally invasive coronary artery bypass grafting. Dual-center experience in 450 consecutive patients. Circulation, 120:S57-S84, 2009.
3) Lapierre H, Chan V, Shomer B, et al.: Minimally invasive coronary artery bypass grafting via a small thoracotomy versus off-pump:a case-matched study. Eur J Cardiothorac Surg, 40: 804-810, 2011.
4) Guo MH, Vo TX, Horsthuis K, et al.: Durability of minimally invasive coronary artery bypass grafting. J Am Coll Cardiol, 78: 1390-1391, 2021.
5) Ruel M, Shariff MA, Lapierre H, et al.: Results of the minimally invasive coronary artery bypass grafting angiographic patency study. J Thorac Cardiovasc Surg, 147: 203-209, 2014.
6) Kikuchi K, Une D, Endo Y, et al.: Minimally invasive coronary artery bypass grafting using bilateral in-situ internal thoracic arteries. Ann Thorac Surg, 100: 1083-1084, 2015.
7) Tachibana K, Kikuchi K, Narayama K, et al.: Minimally invasive coronary artery bypass grafting with ultrasonically skeletonized internal thoracic artery. JTCVS Tech, 14: 107-113, 2022.
8) Nambiar P, Mittal C: Minimally invasive coronary bypass using internal thoracic arteries via a left minithoracotomy:“Nambiear Technique”. Innovations, 8: 420-426, 2013.
9) Babliak O, Demianenko V, Melnyk Y, et al.: Complete coronary revascualization via left anterior thoracotomy. Innovations, 14: 330-341, 2019.
10) Giambruno V, Chu MW, Fox S, et al.: Robotic-assisted coronary artery bypass surgery:an 18-year single-centre experience. Int J Med Robot, 14:e1891, 2018.
11) Balkhy HH, Nisivaco S, Kitahara H, et al.: Robotic off-pump totally endoscopic coronary artery bypass in the current era:report of 544 cases. Eur J Cardiothorac Surg, 61: 439-446, 2022.
12) Une D, Lapierre H, Sohmer B, et al. : Can minimally invasive coronary artery bypass grafting be initiated and practiced safely?:a learning curve analysis. Innovations, 8: 403-409, 2013.
13) Patrick WL, Iyengar A, Han JJ, et al.: The learning curve of robotic coronary arterial bypass surgery:a report from the STS database. J Card Surg, 36: 4178-4186, 2021.
14) Panoulas VF, Colombo A, Margonato A, et al.: Hybrid coronary revascularization. Promising, but yet to take off. J Am Coll Cardiol, 65: 85-97, 2015.
15) Shen L, Hu S, Wang H, et al.: One-stop hybrid coronary revascularization versus coronary artery bypass grafting and percutaneous coronary intervention for the treatment of multivessel coronary artery disease. 3-year follow-up results from a single institution. J Am Coll Cardiol, 61: 2525-2533, 2013.
16) Tajstra M, Hrapkowicz T, Hawranek M, et al.: Hybrid coronary revacularization in selected patients with multivessel disease:5-year clinical outcomes of the prospective randomized pilot study. J Am Coll Cardiol Intv, 11: 847-852, 2018.
17) Balkhy HH, Nisivaco S, Kitahara H, et al.: Robotic advanced hybrid coronary revascularization:outcomes with two internal thoracic artery grafts and stents. JTCVS Tech, 16: 76-88, 2022.
18) Kikuchi K, Une D, Suzuki K, et al.: Off-pump minimally invasive coronary artery bypass grafting with a heart positioner:direct retraction for a better exposure. Innovations, 10: 183-187, 2015.
19) Sakaguchi T, Mizuno T, Ryomoto M, et al. : A new multisuction heart positioner for minimally invasive coronary artery bypass grafting. Ann Thorac Surg, 109:e63-e65, 2020.
20) Sakaguchi T, Totsugawa T, Tamura K, et al. : Minimally invasive coronary artery bypass grafting:useful routine option for coronary revascularization in selected cases. Gen Thorac Cardiovasc Surg, 68: 1128-1133, 2020.
PDFを閲覧するためには Adobe Reader が必要です。