日外会誌. 123(3): 228-233, 2022
特集
本邦の大腸癌治療の現状と展望―海外における標準治療と比較して
3.結腸癌の郭清範囲―D3郭清とCME
|
帝京大学医学部附属溝口病院 外科 小林 宏寿 , 高島 順平 , 鈴木 悠太 , 小泉 彩香 , 茂原 富美 , 塚本 充雄 , 山﨑 健司 , 杉本 斉 , 藤本 大裕 , 三浦 文彦 , 谷口 桂三 , 松谷 哲行 |
結腸癌に対する手術の基本は,胎生期の腸回転に伴い周囲組織に固定された腸管および腸間膜を破壊することなく元の固定されていない状態に戻す,いわゆるmesocolic planeでの剥離・授動とともに,支配血管を根部で結紮・切離する中枢方向のリンパ節郭清にある.本邦では従来より腸管切離長に関しては口側・肛門側ともに10cm程度で十分とされてきた一方,最近海外で広く行われつつあるcomplete mesocolic excision with central vascular ligationでは,D3郭清における腸管切離長の約1.5~2.5倍の腸管を切離しており,両者は腸管切離長において大きく異なる術式であることを認識する必要がある.
キーワード
結腸癌, リンパ節郭清, D3郭清, CME
I.はじめに
大腸癌に対する手術の基本は,胎生期の腸回転に伴い周囲組織に固定された腸管および腸間膜を破壊することなく元の固定されていない状態に戻すとともに,支配動脈を根部で結紮・切離し,腫瘍ならびに領域リンパ節をen blocに摘出することにある.
本邦においては進行大腸癌に対してD3リンパ節郭清を伴う腸管切除術が標準術式として行われてきた.本邦における大腸癌の治療成績は良好であり,一般的に結腸癌の治療成績は直腸癌より良好である1).
一方,海外では1980年代にHealdらによって直腸癌に対する標準的術式としてtotal mesorectal excision(TME)が提唱され広く行われる一方で2),結腸癌に対する標準術式として定まったものはなかった.そのため,TMEの採用により直腸癌に対する治療成績が向上する一方で,結腸癌に対する治療成績は長年向上せず,直腸癌の治療成績が結腸癌の治療成績よりも良好となる現象まで出現した3)4).このような背景の下,2000年代後半にドイツErlangen大学のHohenbergerらによってcomplete mesocolic excision with central vascular ligation(CME+CVL)という術式が提唱された5).結腸癌に対するCME+CVLは非常に良好な治療成績を示すことで,その後,多くの施設で行われるようになった.
本稿では本邦で広く行われている結腸癌に対するD3郭清と海外を中心に行われているCME+CVLについて概説するとともに,その相違について述べる.
II.大腸癌におけるD3郭清の歴史
大腸癌治療ガイドラインでは,術前・術中診断にてリンパ節転移を疑う症例や深達度T3以深の症例に対してはD3郭清が推奨されている6).本邦における大腸癌に対するD3郭清の普及には,二つの転機が存在する.
第一に,大腸癌取扱い規約の出版である.大腸癌に対するD3郭清を伴う根治切除術は1970年代以降広く行われるようになってきたが,その普及には大腸癌取扱い規約の出版が大きな役割を果たした7).安富らは「結腸は所属リンパ節を含めて本当の意味でのen-bloc郭清が可能な臓器であって,大腸癌取扱い規約の普及により主幹動脈根までの郭清と十分な腸切除が手術の基本となっている.」と40年近く前に述べている8).
第二に,大腸癌治療ガイドラインの出版である.2005年7月に最初の大腸癌治療ガイドラインが出版され9),その目的として「大腸癌の標準的な治療方針を示すこと」「大腸癌治療の施設間格差をなくすこと」「過剰診療・治療,過小診療・治療をなくすこと」等が挙げられている.当時の大腸癌治療に対する印象は,大学病院や専門施設ではD3郭清が標準的に行われているものの,市中の一般病院では行われていない場合もまだ多いというものであった.Ishiguroらは,2001年から2010年に手術を受けた大腸癌46,304例を検討し,D3郭清の施行率を明らかにしている10).2001年に58.4%だったD3郭清の比率は,2010年には75.0%に上昇していた.特に大腸癌治療ガイドライン出版の前後で比較すると,2001年から2005年でのD3郭清の施行率は2.5%の上昇だったのに対し,2005年から2010年では14.1%上昇していた.
III.結腸癌におけるD3郭清の範囲と治療成績
D3郭清とは腸管傍リンパ節,中間リンパ節および主リンパ節が郭清された状態と定義される.結腸の主幹動脈は,回結腸動脈,右結腸動脈,中結腸動脈(右枝・左枝),左結腸動脈,S状結腸動脈である.腸管傍リンパ節の範囲は一般的に口側,肛門側ともに10cmとされるが,正確には腫瘍と支配動脈の位置関係から以下の四つに分類される11).
1.支配動脈が腫瘍直下にある場合は,腫瘍辺縁から口側,肛門側ともに10cmまでの範囲.
2.支配動脈が腫瘍辺縁から10cm以内に1本ある場合は,支配動脈側は動脈流入部を越えて5cmまで,反対側は腫瘍辺縁から10cmまでの範囲.
3.支配動脈が腫瘍辺縁から10cm以内に2本ある場合は,口側,肛門側ともに支配動脈流入部を越えて5cmまでの範囲.
4.支配動脈が腫瘍辺縁から10cm以内に無い場合は,腫瘍辺縁から最も近い動脈を越えて5cmまで,反対側は腫瘍辺縁から10cmまでの範囲.
ここで改めて述べるまでもないが,D3郭清では前述の範囲にある領域リンパ節は腫瘍を含む腸管とともにen blocに摘出する必要がある.そのため,大前提として腫瘍を含む腸管ならびに腸間膜を損傷することなく,発生学的に正しい剥離層に沿って周囲の組織から授動することもD3郭清の概念には含まれる.
多施設による後方視的観察研究で結腸癌(直腸S状部癌を含む)3,583例を検討したところ,Stage Ⅰ,Ⅱ,Ⅲ結腸癌における治癒切除後の再発率は各々2.7%,12.1%,24.3%であった1).局所再発率は1.8%,吻合部再発は0.3%であり,補助化学療法を行っていない1991年~1996年の症例が対象であることを考えると良好な治療成績といえる.
JCOG0404はStage Ⅱ,Ⅲ症例を対象とした,腹腔鏡下手術の開腹手術に対する非劣性を証明するためのランダム化比較試験である12).5年全生存率は開腹手術群が90.8%,腹腔鏡下手術群が91.8%であった.主要評価項目である生存率の非劣性は示されなかったものの,いずれのアプローチにおいても結腸癌(直腸S状部癌を含む)におけるD3郭清の治療成績は良好といえる.
IV.CME+CVLの手技
2009年にHohenbergerらが提唱したCME+CVLという術式は,すでにD3郭清が標準となっていた本邦においては目新しい概念ではなかった.しかしながら,中枢方向のリンパ節郭清を標準としていなかった諸外国では,大きなインパクトをもって受け入れられた.当時のヨーロッパでは,辺縁動脈に沿ってD3郭清より広範な腸管切除を行う一方,中枢方向のリンパ節郭清に関しては支配血管を根部ではなく,より末梢で切離する術式が一般的であった13).
CMEの基本的なコンセプトは,鋭的剥離により腸管および腸間膜を完全な状態で周囲より授動し,支配血管を根部で切離することと述べられている5).
右側結腸癌の場合,Kocher授動を用いて十二指腸および膵頭部,腸間膜を上腸間膜動脈まで授動する.続いて結腸間膜と膵・十二指腸の間を剥離し,結腸間膜基部すなわち上腸間膜動静脈に到達できるようにする.血管処理は回結腸動静脈から行い,中結腸動静脈に至る.盲腸癌および上行結腸癌では中結腸動静脈の右枝のみ切離し,肝弯および右側横行結腸癌では根部で処理する.ただ,以前ノルウェーで開催されたコンセンサスミーティングでヨーロッパの外科医と話した際には,上行結腸癌では殆どの症例で中結腸動静脈は根部で処理している印象であった.
左側結腸癌では,脾弯の授動を行うとともに左側結腸を授動する.癌の占居部位が左側横行結腸の場合,基本的に中結腸動静脈を根部で切離する.そのため,肝弯を含めた右側結腸の授動を要するとともに,腸管の口側切離部位は上行結腸となる.癌の占居部位が下行結腸中央よりS状結腸にかけての場合は,下腸間膜動脈は根部で処理し,下腸間膜静脈は膵下縁で切離する.下腸間膜動脈を根部で切離するため,肛門側腸管の切離部位は直腸となる.
V.CME+CVLの治療成績
Hohenbergerらは1978年~2002年の治療成績として,Stage Ⅰ,Ⅱ,Ⅲ手術例の局所再発率が0.4%,2.0%,11.1%であったと報告している5).また年代別に局所再発率を検討すると1978年~1984年症例で6.5%であったものが,1995年~2002年症例では3.6%まで減少していた.癌関連生存率はStage Ⅰ,Ⅱ,Ⅲ症例において,各々99.1%,91.4%,70.2%であった.このような良好な治療成績が驚きをもって受け止められ,多くの施設で導入されていった.
BertelsenらはデンマークにおけるCME+CVL導入前後における結腸癌の治療成績について報告している14).2008年から2011年に治癒切除を行ったStage Ⅰ,Ⅱ,Ⅲ症例における4年無病生存率は,CME導入前後で89.8%から100%,77.9%から91.9%,67.5%から73.5%へと上昇していた.
Gaoらは前向きにCMEの有用性について検討している15).2012年から2016年に治療したCME群110例と非CME群を比較したところ,3年局所無再発生存率はCME群で100%,非CME群で90.2%とCME群で有意に良好であった(P<0.001).一方,術後合併症は両群間に差を認めず,ランダム化試験ではないもののCMEが局所制御に有用であるとしている.
VI.D3郭清とCMEの違い
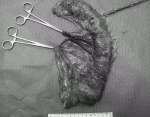
HohenbergerらがCME+CVLを提唱し始めた頃には,D3郭清との違いは明らかではなかった.当初はそのコンセプトからD3郭清と同一のようにも思われた.そこでCME+CVLとD3郭清について比較・検討することとなった16).方法としては日本の2施設でD3郭清を施行した症例とHohenbergerの所属するErlangen大学でCME+CVLを施行した症例の切除標本写真を,切除後すぐに自然な状態で表裏1枚ずつ撮影し比較した(図1).撮影した標本写真は,第3者である英国Leeds大学の病理医により評価された.評価項目は剥離層,ならびに腸管切離長や腫瘍・腸管から支配血管切離部位までの距離,腸間膜面積等であった.剥離層はmesocolic plane,intramesocolic plane,muscularis propria planeに分類し,前者より順に優れた剥離層とした.
剥離層に関してはいずれの群もmuscularis propria planeの手術はなく,mesocolic planeの手術はCME+CVL群88%,D3群73%で行われていた.腸管の切離長はCME+CVL群で有意に長かったものの,腸管から支配血管結紮点までの距離は両群間に差はなかった(表1).腸管切離長を反映して,切除した腸間膜面積はCME+CVL群で有意に広かった.摘出したリンパ節個数については,CME+CVL群で有意に多くなっていたが,転移陽性リンパ節個数については両群間に差を認めなかった.lymph node ratioについても両群間に差を認めなかった.
以上より,CME+CVL群とD3郭清はいずれも発生学的に正しい剥離層に沿った授動が行われており,中枢方向の郭清についてほぼ同様に行われている一方,腸管切離長は右側結腸から横行結腸では約1.5倍,左側結腸では約2.5倍CME+CVL群で長いことが明らかとなった.

VII.今後の展望
適切な剥離層に沿った腸管の授動ならびに支配血管を根部で結紮・切離する中枢方向のリンパ節郭清の重要性について異論はないと思われる.一方,適切な腸管切離長については未だ十分に明らかにされていない.現在,大腸癌研究会のプロジェクト研究「結腸癌の至適腸管切離長に関する前向き研究」(T-REX study)が進行中であり17),結腸癌における適切な切離長が明らかになることが期待される.また,海外ではRELARC trial18)やCOLD trial19)などD2郭清とD3郭清を比較する臨床試験が進行中であり,中枢方向のリンパ節郭清についても新たな知見が得られる可能性があり,興味深い.
VIII.おわりに
本邦で進行結腸癌に対して標準的に行われているD3郭清と海外で徐々に広まりつつあるCME + CVLについて概説した.両者の基本的なコンセプトは近いものの,腸管切離長については大きな隔たりがあり,両者は異なることを認識する必要がある.
利益相反:なし
文献
1) Kobayashi H, Mochizuki H, Sugihara K, et al.: Characteristics of recurrence and surveillance tools after curative resection for colorectal cancer:a multicenter study. Surgery, 141: 67-75, 2007.
2) Heald RJ, Husband EM, Ryall RD: The mesorectum in rectal cancer surgery--the clue to pelvic recurrence? Br J Surg, 69: 613-616, 1982.
3) Birgisson H, Talback M, Gunnarsson U, et al.: Improved survival in cancer of the colon and rectum in Sweden. Eur J Surg Oncol, 31: 845-853, 2005.
4) Iversen LH, Norgaard M, Jepsen P, et al.: Trends in colorectal cancer survival in northern Denmark:1985-2004. Colorectal Dis, 9: 210-217, 2007.
5) Hohenberger W, Weber K, Matzel K, et al.: Standardized surgery for colonic cancer:complete mesocolic excision and central ligation--technical notes and outcome. Colorectal Dis, 11: 354-364; discussion 364-365, 2009.
6) 大腸癌研究会編:大腸癌治療ガイドライン 医師用 2019年版.金原出版,東京,2019.
7) 大腸癌研究会編:大腸癌取扱い規約 初版.金原出版,東京,1977.
8) 安富 正幸,泉本 源太郎,西山 真一:大腸癌手術におけるリンパ節郭清と補助化学療法.日消外会誌,17: 821-825, 1984.
9) 大腸癌研究会編:大腸癌治療ガイドライン 医師用 2005年版.金原出版,東京,2005.
10) Ishiguro M, Higashi T, Watanabe T, et al.: Changes in colorectal cancer care in japan before and after guideline publication:a nationwide survey about D3 lymph node dissection and adjuvant chemotherapy. J Am Coll Surg, 218: 969-977 e1, 2014.
11) 大腸癌研究会編:大腸癌取扱い規約.第9版.金原出版,東京,2018.
12) Kitano S, Inomata M, Mizusawa J, et al.: Survival outcomes following laparoscopic versus open D3 dissection for stage II or III colon cancer (JCOG0404):a phase 3, randomised controlled trial. Lancet Gastroenterol Hepatol, 2: 261-268, 2017.
13) Kobayashi H, West NP, Takahashi K, et al.: Quality of surgery for stage III colon cancer:comparison between England, Germany, and Japan. Ann Surg Oncol, 21 (Suppl 3):S398-S404, 2014.
14) Bertelsen CA, Neuenschwander AU, Jansen JE, et al.: Disease-free survival after complete mesocolic excision compared with conventional colon cancer surgery:a retrospective, population-based study. Lancet Oncol, 16: 161-168, 2015.
15) Gao Z, Wang C, Cui Y, et al.: Efficacy and Safety of Complete Mesocolic Excision in Patients With Colon Cancer:Three-year Results From a Prospective, Nonrandomized, Double-blind, Controlled Trial. Ann Surg, 2018.
16) West NP, Kobayashi H, Takahashi K, et al.: Understanding optimal colonic cancer surgery:comparison of Japanese D3 resection and European complete mesocolic excision with central vascular ligation. J Clin Oncol, 30: 1763-1769, 2012.
17) Shiozawa M, Ueno H, Shiomi A, et al.: Study protocol for an International Prospective Observational Cohort Study for Optimal Bowel Resection Extent and Central Radicality for Colon Cancer (T-REX study). Jpn J Clin Oncol, 51: 145-155, 2021.
18) Xu L, Su X, He Z, et al.: Short-term outcomes of complete mesocolic excision versus D2 dissection in patients undergoing laparoscopic colectomy for right colon cancer (RELARC):a randomised, controlled, phase 3, superiority trial. Lancet Oncol, 22: 391-401, 2021.
19) Karachun A, Panaiotti L, Chernikovskiy I, et al.: Short-term outcomes of a multicentre randomized clinical trial comparing D2 versus D3 lymph node dissection for colonic cancer (COLD trial). Br J Surg, 107: 499-508, 2020.
PDFを閲覧するためには Adobe Reader が必要です。