日外会誌. 122(5): 468-475, 2021
特集
大動脈弁疾患に対する外科的治療の現況
6.TAVIの現況と中期成績
|
慶應義塾大学医学部 循環器内科 林田 健太郎 |
近年本邦においても大動脈弁狭窄症に対する低侵襲治療として経カテーテル的大動脈弁留置術(TAVI)が急速に普及している.2020年には本邦と米国のガイドラインが改訂されており,また低リスク症例におけるTAVIの適応も世界中で承認された.さらに2021年には血液透析患者に対するTAVIの適応も承認されている.一方で生体弁の長期の耐久性や術後抗血栓療法など未解決の課題も存在しており,適応は慎重に判断していくべきである.SAVRとTAVIが補完的に機能することにより,最善の臨床成績が得られると考えられる.
キーワード
TAVI, SAVR, 大動脈弁狭窄症, 低リスク, 血液透析
I.はじめに
経カテーテル的大動脈弁留置術(Transcatheter aortic valve implantation, TAVI)は,周術期リスクが高く外科的大動脈弁置換術(SAVR)の適応とならない高リスクな大動脈弁狭窄症(AS)患者群に対して,開胸や人工心肺を必要としない,より低侵襲な治療として開発されてきた.2002年にフランスのRouen大学のインターベンション医であるAlain Cribier教授によって第1例が施行されて以来1),2007年にはヨーロッパでCEマーク取得,2011年には米国でFDA承認を受け,現在までに欧米を中心に世界中で30万例以上が治療されている.本邦においても2013年より保険償還が得られ,現在189施設(2021年5月現在)が認定されており,急速に普及しつつある.本稿ではこの治療の現状と中期成績について概説していく.
II.適応の変遷―中等度-低リスク患者におけるTAVIとSAVR―
当初TAVI治療の適応は,ASに対する標準治療として確立されてきたSAVRが施行不可能,もしくは高リスクの有症候性重症AS症例に限られており,このように外科周術期リスクスコアは常にgate keeperとして考えられてきた.当初は高リスク症例における無作為化比較試験(RCT)であるPARTNER 1試験やCoreValve高リスク試験の結果に基づきTAVIの適応が決定されてきた.その後TAVI治療技術の進歩や成績の改善に伴い,より低リスク症例へ適応が拡大されてきた.
その後2017年に中等度リスクにおける二つのRCTであるバルーン拡張型弁を使用したPARTNER 2試験や自己拡張型弁を使用したEvolut intermediate risk試験が行われ,短期から中期の成績においてTAVIはSAVRに対し非劣性,もしくは優位性を示した2)
3).以上より2017年に発表された米国のガイドラインでは中等度リスクに対してTAVIの適応が拡大され4),また同年に発表されたESC-EACTSのガイドラインでは中等度リスク患者に対するTAVIがclassⅠとなり,STSスコアが4以上,年齢が75歳以上などがTAVI favorの因子であることが記載された5).
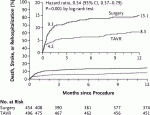
さらに2019年には低リスク患者におけるTAVI とSAVRを比較する二つのRCTが発表されたが,これらの試験には少数例ながら本邦からの患者群もエンロールされた.Sapien 3を用いたPARTNER 3試験では,primary endpointである一年におけるcomposite endpoint(総死亡,脳梗塞,再入院)においてTAVIはSAVRに比べ有意に低く(図1)6),また自己拡張型弁でもTAVIのSAVRに対する非劣勢が証明された7).さらに両試験における術後30日時点での死亡+脳梗塞の頻度はどちらのデバイスを用いても有意にTAVI群が低いことが示された.つまり低リスク患者においても短~中期のhard endpointはSAVRに比べTAVIの方が低いことが複数のRCTによって示された.
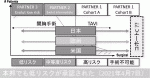
これらの結果をもって2019年には米国,欧州両方で,2021年には本邦においても低リスク患者に対するTAVIの適応が承認された(図2).
またガイドラインとしてはまず2020年3月に本邦において日本循環器学会の弁膜症治療ガイドラインが改訂(後述)され8),その後同年12月に米国のガイドラインが改訂されたが9),低リスク試験の結果を踏まえ,いずれも外科周術期リスクスコアがgate keeperとしては扱われなくなっているのが特徴的である.
III.本邦における弁膜症治療ガイドラインの改訂
2020年3月に日本循環器学会の弁膜症治療ガイドラインが改訂された8).筆者も班員の末席に名を連ねさせていただいたが,いくつかの重要改訂ポイントが挙げられる.
まず外科治療・カテーテル治療の適応と選択について,「年齢,個々の外科弁・TAVI弁の耐久性データ,SAVR手技リスク,TAVI手技リスク,解剖学的特徴,併存疾患,フレイル,同時に必要な手技を鑑みる」ことが記載されている.弁膜症チームで協議すべき因子として表1が記載されているが,これはESC/EACTSガイドラインを模して作成しているものの,こちらから外科周術期リスクスコアが削除されたのが特徴的である.よりTAVIリスクが高ければSAVR,SAVRリスクが高ければTAVIを選択し,両方の手技リスクが低ければ,年齢,フレイル,併存疾患,同時に施行すべき手技(CABGなど),などを含めて決定することが要旨である.特にTAVIにおいてはTFアプローチで安全に施行できることが重要であると考えられている.実際本邦における単独SAVRの30日死亡率は1.9%,再手術群では5.0%と大変良好な成績が得られている10).一方TAVIがより高齢で再手術を含むリスクの高い患者群を対象としているにも関わらず,30日死亡率2%以下とさらに良好な成績が報告されている11)
12).
また低リスク患者において,TAVIはSAVRに比べ長期予後のデータはないが,中期成績においては同等かより良好,短期成績ではより良好であることが複数のRCTによって示されている.TAVI弁の耐久性についてもいくつか報告があり,10年以下の耐久性はSAVR弁と遜色ない結果を示しているが,10年以上のデータについてはいまだ乏しいこと,また耐久性の課題があるため若年者にはTAVIの適応を注意すべきであり,また寝たきり,認知症患者への安易な介入は厳に慎むべきである.倫理的かつ医療経済的観点も十分に考慮して,弁膜症チームで慎重に協議したうえで適応を決定すべきである旨が記載されている.実際われわれはフレイルの強い患者や認知症が高度な患者にTAVIを施行しても予後が悪いことを報告しており13)
14),患者選択には細心の注意が必要である.また年齢の基準についても科学的根拠はあまり存在せず,ESC/EACTSのガイドラインでは75歳がSAVR/TAVI選択のカットオフであったこと,本邦では高齢者の平均寿命が欧米と比べ3~5歳長く,またある年齢における平均余命は1~2歳長いことが知られているため,最終的に大まかな目安として75歳以下をSAVR favor,80歳以上をTAVI favorとしている.さらに「全てのAS患者に対しSAVR,TAVI両方の治療について,十分な最新の情報に基づく正しいインフォームドコンセントがなされるべきである.個々の患者の価値観や希望も加味した上で,最終的には弁膜症チームでの議論を経て決定されるべきである」と記載されているが,本邦のTAVI施設基準がハイブリッド手術室や外科専門医3人など比較的高い施設基準を満たす必要がある中,TAVIを施行していない外科施設においてはなかなか満たすことが難しいのが現状ではないかと推測される.

IV.今後の課題
従来TAVIの大きな課題とされてきた弁周囲逆流や血管合併症はデバイスの改良やスクリーニングの改善により,克服されつつある.また従来適応とされていなかった二尖弁に対しても近年最新デバイスを使用することによる弁周囲逆流が減少し,非二尖弁症例と同様な成績が達成できるということが報告されている15).
最大の焦点となりうるのは弁の耐久性だが,現在最長10年間までの耐久性データが存在しており16)
17),10年における再治療回避率は93.5%と限られた症例数ながら比較的良好な成績を示している.また中等度リスク患者におけるPARTNER 2試験の5年成績において,第二世代デバイスであるSapien XTはSAVRに比べ有意に弁の劣化が多かったが,現在使用している第三世代デバイスであるSapien 3はSAVRと有意差は認めず同等であった18).また北欧で行われた低リスク患者に対するSAVRとTAVIのRCTであるNOTION trialでは5年の成績が報告されているが,SAVR弁に比べTAVI弁の方が弁の劣化(structural valve deterioration, SVD)が少なかったという結果であった19).これはSVDの定義や外科弁の選択(Mosaic:27%,Epic:29%,Trifecta:24%,Perimount:10%,Sorin Mitroflow:10%)が影響していると考えられる.今後より多数例におけるより長期の耐久性データが,今後若年者に対して適応を拡大していくには必要となるであろう.特に米国で昨年発表された弁膜症治療ガイドラインでは,65歳以下をSAVR,65~80歳ではSAVR, TAVIともにclassⅠ,80歳以上ではTAVIがclassⅠ,SAVRがclassⅡaの適応とされている9).現在のTAVI弁の耐久性データを鑑み,また劣化TAVI弁に対し再度TAVIを施行する“TAV in TAVまたはre-do TAVI”20)が薬事承認されていない本邦においてはやや時期尚早であり,なかなかそのまま適応し難いのではないかと考えられる.
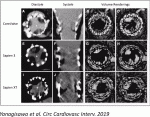
また術後造影CTを撮影すると血栓が付着する現象が報告されており21),外科弁に比べTAVI弁で頻度が多いことが知られている.この現象が長期の生体弁の耐久性に与える影響についてはいまだ明らかになっていない.われわれも本邦のTAVI患者において同様の血栓が認められることを報告した(図3)22).
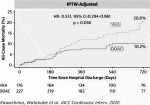
従来TAVI術後の抗血栓療法としてはDAPTが標準的であったが,近年DAPTに比べASA単剤の方が出血性イベントの減少と予後の改善がみられることが報告された(POPular-TAVI,cohort A)23),また抗凝固が必要な症例については,抗凝固+Clopidogrelに比べ抗凝固単剤の方が予後が良いことも発表された(POPular-TAVI,cohort A)24).以上より,TAVI後は抗血栓療法はなるべく少なめの方が出血イベントを減少させ総死亡を低下させることがわかり,高齢かつ高リスク患者の多く含まれるTAVI患者においては納得できる結果となった.また抗凝固においてWarfarinよりDOACの方が総死亡を低下させることをわれわれはOCEAN-TAVI registryより発表しており(図4)25),今後前向きのRCTであるENVISAGE-TAVI AF試験(NCT02943785)の結果が2021年中に発表される予定である.
さらに従来本邦では血液透析患者がTAVIの適応外とされてきたが,外科周術期リスクも比較的高く26),TAVIの適応拡大が期待されてきた.2015年より大阪大学と慶應義塾大学の2施設で治験を行い,ようやく2021年1月に血液透析患者に対するTAVIが薬事承認された.現在国内約30施設で血液透析患者に対するTAVIが施行できるが,通常の患者と比べ全身の石灰化が強く合併症が発生しやすい可能性があり,また感染性心内膜炎のリスクも上昇することが知られている.さらに弁の劣化も起きやすく,適応や手技には注意が必要である.
またTAVI患者は高齢であり認知機能が年齢相応に低下している場合が多く適応判断に迷う場合が多いが,家族のサポート,医療スタッフによる本人や家族の理解の確認も含めて慎重な判断が必要である.
さらに併存疾患(例えば悪性腫瘍など)が存在し,一年以上の予後が見込まれない場合には,通常このような侵襲的治療の適応とならないと考えられている.このようなTAVIによっても予後が改善されない患者群(futile, cohort C)をいかに同定し,適応を慎重に検討していくことが今後成績のさらなる改善,医療資源の適切な配分に重要であろう.
さらにSAVRとTAVIをうまく組み合わせて治療選択をしてくことで,それぞれの成績を向上させていくことが可能であると考えられている.実際本邦における外科データベースから,SAVRの周術期死亡率をTAVI施設と非TAVI施設で比較すると有意にTAVI施設の方が低かったという報告がされている27).この二つの侵襲的治療法はお互いを侵食するものではなく,相互に補完的に働き結果的にAS患者の治療成績を向上させることが示唆された.今後非TAVI施設においてもTAVI施設との連携などを通して,国内のどの地域においても患者により均一な医療を提供していけるスキームを検討していくべきと考えられる.
V.おわりに
本稿ではTAVIの現状と中期成績について概説した.比較的短期間で成績が確立し,適応が年々拡大しておりパラダイムシフトが生じている.一方でまだ解決されていない課題も残っており,今後さらなる経験やデータの蓄積,デバイスの進化が求められている.またこの低侵襲治療の発展により,SAVRにおいてもMICSの発展など相互作用が生じ,お互い切磋琢磨することにより治療全体の質が向上していることが考えられる.特に高齢かつ高リスクなTAVI患者がTAVI不適となった場合,最後の砦はSAVRとなるため,外科医のより確かな技術と経験が必要不可欠となってくる.またTAVIに興味を持ち実際にTF-TAVIの手技をする外科医が増えてきており,大変嬉しく思っている.われわれインターベンション医も外科医の良きパートナーとして,共通の目標であるより良い医療を提供し末永く共に治療にあたっていきたいと考えている.
利益相反
その他報酬:エドワーズライフサイエンス株式会社,日本メドトロニック株式会社
文献
1) Cribier A , Eltchaninoff H , Bash A , et al.: Percutaneous transcatheter implantation of an aortic valve prosthesis for calcific aortic stenosis:first human case description. Circulation, 106(24): 3006-3008, 2002.
2) Leon MB , Smith CR , Mack MJ , et al.: Transcatheter or Surgical Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med, 374(17): 1609-1620, 2016.
3) Reardon MJ , Van Mieghem NM , Popma JJ , et al.: Surgical or Transcatheter Aortic-Valve Replacement in Intermediate-Risk Patients. N Engl J Med, 376(14): 1321-1331, 2017.
4) Nishimura RA , Otto CM , Bonow RO , et al.: 2017 AHA/ACC Focused Update of the 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease:A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. J Am Coll Cardiol, 135:e1159-e1195, 2017.
5) Baumgartner H , Falk V , Bax JJ , et al.: 2017 ESC/EACTS Guidelines for the management of valvular heart disease:The Task Force for the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J, 38: 2739-2791, 2017.
6) Mack MJ , Leon MB , Thourani VH , et al.: Transcatheter Aortic-Valve Replacement with a Balloon-Expandable Valve in Low-Risk Patients. N Engl J Med, 380: 1695-1705, 2019.
7) Popma JJ , Deeb GM , Yakubov SJ , et al.: Transcatheter Aortic-Valve Replacement with a Self-Expanding Valve in Low-Risk Patients. N Engl J Med, 380: 1706-1715, 2019.
8) Izumi C , Eishi K , Ashihara K , et al.: JCS/JSCS/JATS/JSVS 2020 Guidelines on the Management of Valvular Heart Disease. Circ J, 84(11): 2037-2119, 2020.
9) Otto CM , Nishimura RA , Bonow RO , et al.: 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: Executive Summary:A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 143(5):e35-e71, 2021.
10) Committee for Scientific Affairs TJAfTS, Shimizu H , Endo S , et al.: Thoracic and cardiovascular surgery in Japan in 2016 : Annual report by The Japanese Association for Thoracic Surgery. Gen Thorac Cardiovasc Surg, 67(4): 377-411, 2019.
11) Handa N , Kumamaru H , Torikai K , et al.: Learning Curve for Transcatheter Aortic Valve Implantation Under a Controlled Introduction System ― Initial Analysis of a Japanese Nationwide Registry ―. Circulation Journal, 82: 1951-1958, 2018.
12) Yamamoto M , Watanabe Y , Tada N , et al.: Transcatheter aortic valve replacement outcomes in Japan:Optimized CathEter vAlvular iNtervention (OCEAN) Japanese multicenter registry. Cardiovasc Revasc Med, 20(10): 843-851, 2019.
13) Shimura T , Yamamoto M , Kano S , et al.: Impact of the Clinical Frailty Scale on Outcomes After Transcatheter Aortic Valve Replacement. Circulation, 135(21): 2013-2024, 2017.
14) Yanagisawa R , Tanaka M , Yashima F , et al.: Frequency and Consequences of Cognitive Impairmentin Patients Underwent Transcatheter Aortic Valve Implantation. Am J Cardiol, 122(5): 844-850, 2018.
15) Yoon SH , Bleiziffer S , De Backer O , et al.: Outcomes in Transcatheter Aortic Valve Replacement for Bicuspid Versus Tricuspid Aortic Valve Stenosis. J Am Coll Cardiol, 69(21): 2579-2589, 2017.
16) Deutsch MA , Erlebach M , Burri M , et al.: Beyond the five-year horizon:long-term outcome of high-risk and inoperable patients undergoing TAVR with first-generation devices. EuroIntervention, 14(1): 41-49, 2018.
17) Sathananthan J , Lauck S , Polderman J , et al.: Ten year follow-up of high-risk patients treated during the early experience with transcatheter aortic valve replacement. Catheter Cardiovasc Interv, 97(3):E431-E437, 2021.
18) Pibarot P , Ternacle J , Jaber WA , et al.: Structural Deterioration of Transcatheter Versus Surgical Aortic Valve Bioprostheses in the PARTNER-2 Trial. J Am Coll Cardiol, 76(16): 1830-1843, 2020.
19) Sondergaard L , Ihlemann N , Capodanno D , et al.: Durability of Transcatheter and Surgical Bioprosthetic Aortic Valves in Patients at Lower Surgical Risk. J Am Coll Cardiol, 73(5): 546-553, 2019.
20) Landes U , Webb JG , De Backer O , et al.: Repeat Transcatheter Aortic Valve Replacement for Transcatheter Prosthesis Dysfunction. J Am Coll Cardiol, 75(16): 1882-1893, 2020.
21) Makkar RR , Fontana G , Jilaihawi H , et al.: Possible Subclinical Leaflet Thrombosis in Bioprosthetic Aortic Valves. N Engl J Med, 373(21): 2015-2024, 2015.
22) Yanagisawa R , Tanaka M , Yashima F , et al.: Early and Late Leaflet Thrombosis After Transcatheter Aortic Valve Replacement. Circ Cardiovasc Interv, 12(2):e007349, 2019.
23) Brouwer J , Nijenhuis VJ , Delewi R , et al.: Aspirin with or without Clopidogrel after Transcatheter Aortic-Valve Implantation. N Engl J Med, 383(15): 1447-1457, 2020.
24) Nijenhuis VJ , Brouwer J , Delewi R , et al.: Anticoagulation with or without Clopidogrel after Transcatheter Aortic-Valve Implantation. N Engl J Med, 382(18): 1696-1707, 2020.
25) Kawashima H , Watanabe Y , Hioki H , et al.: Direct Oral Anticoagulants Versus Vitamin K Antagonists in Patients With Atrial Fibrillation After TAVR. JACC Cardiovasc Interv, 13(22): 2587-2597, 2020.
26) Mentias A , Desai MY , Saad M , et al.: Management of Aortic Stenosis in Patients With End-Stage Renal Disease on Hemodialysis. Circ Cardiovasc Interv, 13(8):e009252, 2020.
27) Tabata M , Kumamaru H , Ono A , et al.: The Association of In-Hospital Transcatheter Aortic Valve Replacement Availability on Outcomes of Surgical Aortic Valve Replacement in Elderly Patients. Circ J, 84(9): 1599-1604, 2020.
PDFを閲覧するためには Adobe Reader が必要です。