日外会誌. 125(4): 325-332, 2024
特集
肺癌外科診療up to date
5.小型肺癌に対する縮小手術
|
広島大学 原爆放射線医科学研究所腫瘍外科 見前 隆洋 , 岡田 守人 |
大規模前向き試験,特にJapan Clinical Oncology Group(JCOG)0802/West Japan Oncology Group (WJOG)4607Lの結果から,肺野末梢小型の非小細胞肺癌に対して,縮小手術が積極的適応として選択される機会が増加している.縮小手術には楔状切除と区域切除とコンセプトの異なる術式があり,各術式の目的を十分に理解し適切な縮小手術を選択する必要がある.そのポイントとしてはサージカルマージン確保とリンパ節郭清の必要性が挙げられ,患者背景も考慮するべきである.画像上solid優位な病変の場合,肺門縦隔リンパ節郭清を伴う解剖学的区域切除が適しており,一方で画像上すりガラス影優位な病変の場合は,楔状切除または区域切除(郭清は必ずしも必須ではない)でサージカルマージンを確保できる術式を選択する.また,リスクのある対象や高齢者に関しては,JCOG1708(間質性肺炎合併肺癌),JCOG1909(肺葉切除高リスク患者),JCOG2109(高齢者肺癌)などの試験が進行中であり,適切な術式を検証している.肺実質温存の生存への寄与が明らかとなった現在,肺実質切除量を最小限に抑えるべく,われわれ呼吸器外科医は,腫瘍の評価方法や手技の向上に取り組み,モダリティーの開発などを通して,より多くの患者に対して恩恵の大きい手術提供が可能となるように努めるべきである.
キーワード
楔状切除, 区域切除, リンパ節郭清, Japan Clinical Oncology Group(JCOG), 積極的適応
I.はじめに
近年,縮小手術に関する後ろ向きの結果など1)
~
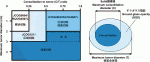
6)に基づいて計画された,Japan Clinical Oncology Group (JCOG) JCOG0802/ West Japan Oncology Group (WJOG)4607L7),JCOG0804/WJOG4507L8),JCOG12119),Cancer and Leukemia Group B (CALGB)14050310)といった大規模前向き試験の結果が続々と明らかとなっている.検診などのスクリーニング11)にて小型肺病変の指摘が多くなされている現在,これらの結果を踏まえて肺野末梢小型の非小細胞肺癌に対して,積極的適応として区域切除や楔状切除といった縮小手術が選択される機会は増加している.しかし,一口に縮小手術と言っても,肺葉切除よりも肺実質切除量が少ない点では一致しているものの,区域切除と楔状切除は難易度やリンパ節郭清における局所制御など全く異なる術式である.つまり,同じ縮小手術とは言えどちらでも良い訳ではなく,術前画像評価および術中所見を踏まえてその腫瘍学的悪性度と局在から適切な術式選択が必要である.特に積極的適応では局所制御が劣ることなく,肺実質切除量を最小限に止めることが肝要である.本稿では,これまでJCOGを中心として本邦で進めてきた縮小手術の治療開発マップ(図1)の基準である病変全体径およびconsolidation to tumor (C/T)比に従って,非小細胞肺癌に対する縮小手術について述べる.また,高齢者における積極的縮小手術や肺葉切除ハイリスク患者に関する消極的縮小手術に関しても言及する.本稿は区域切除や楔状切除を念頭においた内容であり,明らかに肺葉切除以上でなければ完全切除し得ない局在や大きさを示す腫瘍については触れない.
II.縮小手術
縮小手術は「limited resection」とも呼ばれるが,「sublobar resection」という表現も用いられており,これらの用語は肺葉切除を基本とした考えに基づいているものである.楔状切除と区域切除を指すが,はじめに述べたように全く異なる術式である.もう少し詳細に分けると,区域切除にはリンパ節郭清を伴わない楔状切除と同じ,サージカルマージンを確保すれば良いというコンセプトのものと,肺門縦隔リンパ節郭清を伴う解剖学的区域切除に区別される.リンパ節郭清が不要,もしくは何らかの理由で施行しない場合には,サージカルマージン確保ができる術式として楔状切除もしくはリンパ節郭清を省略した区域切除が選択される.特に,やや中枢側に腫瘍が存在する場合には区域切除の良い適応であろう.また,ある程度リンパ節転移の可能性がある腫瘍では,根治性だけでなく正確なステージングの意味でもリンパ節郭清が施行されるべきで,仮にサージカルマージンが楔状切除で確保できるような局在であっても肺門縦隔リンパ節郭清を伴う解剖学的区域切除が適切と言える.リンパ節検索およびサンプリング/郭清において,楔状切除では,特に肺門リンパ節に関しては限界があり,区域切除に有利である.それぞれの術式が選択される目的を十分に理解し,適切な縮小手術が選択される必要がある.
III.小型肺癌に対する多施設共同試験結果
近年の小型肺癌に対する多施設共同研究の結果に関して概説したい.まずは呼吸器外科領域の術式比較試験で世界最大規模のJCOG0802/WJOG 4607L試験7)であるが,肺野末梢に存在する病変全体径2cm以下かつ画像上solid優位な病変を有する患者(85歳以下)が対象である.標準治療の肺葉切除と試験治療の区域切除を比較する試験で,いずれも肺門縦隔リンパ節郭清が必須とされた.主要評価項目である全生存期間において,肺葉切除に対する区域切除の非劣性のみならず優越性が示され,区域切除も本対象の標準治療の一つとなった.術後1秒量の減少率は肺葉切除 -13.1%,区域切除 -10.4%と約3%の差であった.また,Loco-regional recurrenceは肺葉切除 3.1%,区域切除 6.9%であった.類似の試験としてCALGB14050310)がある.北米で行われた試験であるが,病変全体径2cm以下であることは同様であるものの,画像上solid優位かに関しての規定はなく,solid優位な腫瘍が多いとは予想されるが推測の域を出ない.また,試験治療群は縮小手術であり,区域切除のみならず楔状切除も含まれる.加えて,術中に10 番リンパ節と2 ステーションの縦隔リンパ節を迅速病理に提出し,病理学的に転移陰性の確認が必須である点も認識しておくべきである.その上で,主要評価項目の無病生存期間に関して,縮小手術は肺葉切除術に対して非劣性を示した.優越性が示されていないことはJCOG 0802/WJOG4607Lとは異なる結果であり,主要評価項目も異なるため,楔状切除よりも区域切除が良いかどうかに関して今後解決すべき臨床的疑問が残る.術後1秒量の減少率は肺葉切除 -6.0%,区域切除 -4.0%と約2%の差であった.また,Locoregional recurrenceは肺葉切除 12.7%,区域切除 15.3%であった.
上述の対象よりもより低悪性度を示す病変全体径2cm以下かつC/T比 0.25以下の非小細胞肺癌を対象とした縮小手術(楔状切除もしくは区域切除)の前向き試験がJCOG0804/WJOG4507L8)である.10年フォローアップの成績も報告され,10年無再発および全生存割合は98.6% および98.5%と非常に良好な予後を示し,縮小手術が行われた314例(楔状切除 258例,区域切除 56例)のうち局所断端再発は1例のみで認められた.JCOG12119)は少し対象となる腫瘍が大きく,病変全体径3cm以下かつ画像上GGO (ground glass opacity)優位な非小細胞肺癌で,JCOG0804/WJOG4507Lの対象となる病変が除外されたデザインになっており,区域切除単群の検証的試験である.5年無再発および全生存割合は98.0% および98.2%と,この試験でも非常に良好な予後を示した.登録された全396例のうち,Locoregional recurrenceは1例のみであった.
以上を踏まえて,以降ではそれぞれの対象における縮小手術の選択に関して述べる.
IV.画像上solid優位な病変に対する縮小手術
まずはJCOG0802/WJOG4607L試験の対象における縮小手術について述べる.ここでの縮小手術は解剖学的区域切除+肺門縦隔リンパ節郭清である.試験における対象は肺野末梢,つまり外套1/3に存在する病変全体径2cm以下かつC/T比0.5を超える画像上solid優位な病変である.そのため,中枢病変に関しての区域切除には十分なエビデンスがない状況であり,その適応は慎重になるべきである.しかし,切除マージンが確保できると判断される症例においては,中枢病変に対しても区域切除の積極的適応として良いと考えている.また,2cmを超える画像上solid優位な病変への積極的適応は現在の前向き臨床試験(WJOG16923L,JCOG2217)の結果が待たれるところである.
いずれの縮小手術でも言えることであるが,積極的適応である際には特に,肺葉切除を選択していれば避けられた局所再発を生じないように留意しなければならない.JCOG0802/WJOG4607Lの結果を紐解いてみても,肺葉切除していれば防げた局所再発部位の中で,区域切除群に多かったものは区域間切離端および気管支断端再発であり,区域切除を選択・施行の際にはサージカルマージンに最大限の配慮が必要と言える.それを極力最小限に抑える意味で,症例選択や縮小手術の技術向上,切除マージンが十分でない際に術中に適切に肺葉切除へ移行する判断力が重要と言える.もちろん,私たち腫瘍外科医は患者の健康な予後を延長することが最大の目標であることは言うまでもない.しかしながら,局所断端再発時にはcompletion lobectomyといった高侵襲かつ高難度な手術が必要となる可能性があることなどを踏まえると,当然局所断端再発のない手術を追求し,肺温存によるより良好な予後という恩恵を最大限に患者に届けなければならない.
区域切除では肺葉切除と比較してリンパ節郭清が不十分になるのではないかと危惧されることも多い.しかしながら,JCOG0802/WJOG4607Lにおけるリンパ節転移陽性割合は区域切除群と肺葉切除群において肺門リンパ節でも縦隔リンパ節でも同程度であったことから,区域切除のリンパ節評価が肺葉切除に比し不十分にはならないと考えられる.さらに,区域切除で不十分になることが危惧されるのは肺門リンパ節郭清であるが,術後肺門リンパ節再発においても両群間で同程度であり,肺門リンパ節郭清が不十分になることも否定的と言える.縦隔リンパ節転移再発に関しては区域切除群で多い傾向であったが,技術的に区域切除で縦隔リンパ節郭清が施行困難とは考えにくいため,その科学的根拠は不明瞭のままである.
また,JCOG0802/WJOG4607Lのプロトコールに沿うと術前のみならず術中もリンパ節転移の確認が必要と考えられる.一方で,術中や術後にリンパ節転移が判明した場合,術中に肺葉切除へ移行したり,区域切除術後にcompletion lobectomyを施行したりする方が良好な予後が得られるかは議論のあるところである.このような臨床的疑問は今後前向き試験で検証されるのが一番であるが,その対象患者は多いとは言えないため,実現性の点で困難かもしれない.現時点ではリンパ節転移判明時に肺葉切除に移行しないことを強くは勧められないものの,リンパ節転移を理由に肺葉切除に移行する場合,特に術後のcompletion lobectomyにおいては,手術侵襲と局所コントロールのバランスを踏まえた慎重な判断が必要である.
V.画像上すりガラス影優位な病変に対する縮小手術
続いてJCOG0804/WJOG4507L試験およびJCOG 1211試験の対象における縮小手術について述べる.二つの試験を合わせた対象は病変全体径3cm以下かつC/T比0.5以下の画像上GGO優位な病変である.JCOG1211においては,区域切除で完全切除できる中枢病変も対象となっている.もちろん区域気管支の起始部に近接するような病変であれば肺葉切除しなければ完全切除困難であり,症例選択にはやはりマージンへの配慮が必要となる.病変としての悪性度はJCOG0802試験の対象よりも低いものの,触知などで術中に確認することが容易ではなく,実はマージンの確保に関しては画像上GGO優位な腫瘍の方がsolid優位な腫瘍よりも困難な場合がある.
この対象ではリンパ節転移は極めて低頻度である.JCOG1211でも 395例のうち2 例に肺門リンパ節転移を認めたのみであり,縦隔リンパ節転移は認められなかった.また,同側肺門縦隔リンパ節再発は1例のみであった.筆者らが行った神奈川県立がんセンター,東京医科大学,広島大学の3施設のデータベースを用いた解析では,病変全体径3cm以下かつGGO優位な病変の完全切除(肺葉切除,区域切除,もしくは楔状切除)988例において術後永久病理での肺門リンパ節転移は1例のみで縦隔リンパ節転移は認められなかった12).そしてその肺門リンパ節転移症例は腫瘍が中枢に存在するため,肺葉切除が選択されており,転移部位は#13リンパ節と区域切除以上の解剖学的切除では単純切除で自然と採取される部位であった.加えて,観察期間中央値54.5カ月でリンパ節郭清の程度に関わらず術後肺門縦隔リンパ節再発は認められなかった.これらのことから,同対象におけるリンパ節郭清は不要で,腫瘍の局在からマージンが確保できる術式を肺葉切除,区域切除,楔状切除の中から適切に選択をすることが肝要であると言える.
VI.高齢者における縮小手術
本項目においては,いわゆる手術リスクのある高齢者ではなく,耐術能を十分に有する高齢者における積極的適応としての縮小手術に関して述べたい.耐術能の判断で年齢は重要なリスク因子の一つであるが,年齢だけでは測れないことは多くの外科医が認識するところである.高齢化社会が進むにつれて肺癌手術患者の中で高齢者の占める割合は上昇を続けており,70歳以上は60%程度,80歳以上でも15%程度を占めるようになってきた13).年齢というリスクだけを考慮した場合,短期的な耐術能としては肺葉以上の切除が可能な高齢者は一定数存在するが,高齢者には寿命という要因が必ず影響するため,長期的予後を考えた際に,がんの根治性を優先すべきか肺切除量の縮小による術後全身状態を優先すべきか議論がある.先の項目で述べたJCOG0802/WJOG4607L試験では,全生存期間における肺葉切除に対する区域切除の優位性は74歳以下よりも75歳以上において顕著であった.この結果は,高齢であればあるほど肺切除量縮小の生存における恩恵が大きいことを示唆している.また,がんの治療としては大きく切除することが予後改善につながると考えられてきたが,切除区域数が少ないほど術後他病死が少ない傾向にあり(unpublished data),重要なvital organの一つである肺の残存量も予後に多大な影響を与えることが明らかとなった.それを踏まえて,高齢者では全生存期間において劣ることなく区域切除からさらなる肺切除量の縮小(楔状切除)が可能ではないかと考えている.日本呼吸器外科学会学術委員会企画:高齢者肺癌に対する外科治療の安全性と有効性を評価する多施設共同前向き調査研究(JACS1303)の副解析では,病変全体径2cm以下かつC/T比0.5を超える画像上solid優位な病変を有する80歳以上の高齢者において,3年全生存割合は楔状切除:89.4%,区域切除 + 肺葉切除:75.8%と楔状切除で軽度良好(有意差なし,P = 0.14)であった14).区域切除のみに限定した場合(3年全生存割合 85.7%)も楔状切除との予後における関係は同様の傾向であった(表1).また,80歳以上の高齢者においては楔状切除が肺葉切除や区域切除と同程度の予後を示す可能性15)や,高齢者においては若年者よりも肺切除術後の肺機能が予測以上に低下する傾向にあること16),高齢の方が肺切除量の術後他病死における影響が大きい可能性17)が報告されている.ただし,これらは後ろ向きな検討であり,80歳以上のような高齢者において,楔状切除でも標準治療である区域切除と遜色ない生存が期待できるのか,いずれかの縮小手術がより高齢者にとって良いのかに関しては不明である.それを明らかにすべく,現在JCOG2109(AWESOME試験)として前向き試験が進行中であり 18),結果が待たれるところである.また,さらに大きな2~4cmの病変を有する高齢者において,縮小症手術後と肺葉切除後とで同程度の長期予後を示す報告19)もあり,高齢者における縮小手術の積極的適応拡大がどこまで行われるべきか注目される.

VII.手術リスクのある患者における 縮小手術
肺癌に罹患する患者は元来背景肺にリスクを伴うような場合も少なくない.代表的な肺疾患は肺気腫を含む慢性閉塞性肺疾患(chronic obstructive pulmonary disease, COPD)や間質性肺炎である.それに伴い,心肺ともにリスクのあることも多い.そのような患者において最適な術式選択を検証する試験として,JCOGではJCOG1708,JCOG1909として縮小手術に関する試験が行われている.
JCOG1708は間質性肺炎合併肺癌を対象とした試験である.試験の詳細は別に譲るが,肺葉切除は耐術と判断される特発性間質性肺炎合併肺癌患者が対象となっている.標準治療の肺葉切除と試験治療の楔状切除(区域切除を許容)を比較する非劣性試験のデザインである.間質性肺炎急性増悪が肺癌術後周術期死亡の最大の原因として知られており,呼吸機能そのもののみならず,短期的にリスクが大きい.加えて,特発性間質性肺炎患者自体の予後も不良であるため長期的にもリスクが高い.さらに二次肺癌も生じやすいことが知られている.これらのことから,がんの根治性がある程度落ちる可能性があるものの,縮小手術を選択することで総合的に予後が保たれる,もしくは良好な可能性があると考えられる.現在患者登録中であり,間質性肺炎合併肺癌における縮小手術の意義が明らかとなることが期待される.
JCOG1909は肺葉切除高リスクな耐術能を有する肺癌において,いずれも縮小手術である楔状切除(標準治療群)と区域切除(試験治療群)を比較する優越性試験である.こちらも詳細は割愛させていただくが,肺葉切除の耐術能においてリスクが高い場合に,がんの根治性を優先して局所コントロールが優れる区域切除を選択すべきか,術後全身状態を優先した楔状切除を選択すべきかを検証する.手術リスクのある患者における治療開発においては,肺切除量を縮小させる方向に向かう傾向が強いが,この試験では,がんの局所コントロールをしっかりと行うことでより長期の予後を目指す点が特徴的である.どちらの治療を行っても他疾患や寿命で早期に死期を迎えるような患者ではなく,肺葉切除高リスクとはいえ長期生存が望める患者が想定されていると考えられる.また,適格基準からは肺機能が不良な患者が主な対象の一つであり,そのような背景肺に生じる肺癌は高悪性度が予想されることも念頭にあると思われる.結果によって消極的適応における縮小手術の考え方を変えるかもしれない点でも非常に興味深い試験である.
VIII.おわりに
JCOG0802/WJOG4607L,JCOG0804/WJOG4507L,JCOG1211,CALGB140503の結果から,肺癌治療における縮小手術の重要性が示され,改めて治療選択において鍵となる術式であることが認識された.今後は,縮小手術における適切な患者選択においても,薬物療法のように遺伝子変異ステータスやPD-L1など,さまざまな腫瘍のマーカーを参考にしていく可能性もある20).ここまで述べたように,大切なことは腫瘍の状況と患者背景を複合的に判断して,適切な術式選択を行うことであり,それぞれの患者に最適な治療提供がなされなければならない.もちろん,肺葉切除が選択されるべき症例も存在するが,sleeve segmentectomy21)を考慮するなど,安易に肺切除量が増加する選択は避けるべきである.特に,JCOG0802/ WJOG4607Lにより肺実質温存の生存への寄与が明らかとなった現在,肺実質切除量を必要最小限に抑えるべく,その腫瘍の評価方法や手術手技の向上に精進し,3D CT22)をはじめとするモダリティーの開発などの努力を怠らず,より多くの患者に恩恵の大きい手術提供が可能となるようにわれわれ呼吸器外科医は進んでいくべきである.
利益相反:なし
文献
1) Okada M , Koike T , Higashiyama M , et al.: Radical sublobar resection for small-sized non-small cell lung cancer:a multicenter study. J Thorac Cardiovasc Surg, 132: 769-775, 2006.
2) Okada M , Nishio W , Sakamoto T , et al.: Effect of tumor size on prognosis in patients with non-small cell lung cancer:the role of segmentectomy as a type of lesser resection. J Thorac Cardiovasc Surg, 129: 87-93, 2005.
3) Okada M , Mimura T , Ikegaki J , et al.: A novel video-assisted anatomic segmentectomy technique:selective segmental inflation via bronchofiberoptic jet followed by cautery cutting. J Thorac Cardiovasc Surg, 133: 753-758, 2007.
4) Okada M , Tsutani Y , Ikeda T , et al.: Radical hybrid video-assisted thoracic segmentectomy:long-term results of minimally invasive anatomical sublobar resection for treating lung cancer. Interact Cardiovasc Thorac Surg, 14: 5-11, 2012.
5) Okada M , Mimae T , Tsutani Y , et al.: Segmentectomy versus lobectomy for clinical stage IA lung adenocarcinoma. Ann Cardiothorac Surg, 3: 153-159, 2014.
6) Mimae T , Okada M : Are segmentectomy and lobectomy comparable in terms of curative intent for early stage non-small cell lung cancer? Gen Thorac Cardiovasc Surg, 68: 703-706, 2020.
7) Saji H , Okada M , Tsuboi M , et al.: Segmentectomy versus lobectomy in small-sized peripheral non-small-cell lung cancer (JCOG0802/WJOG4607L):a multicentre, open-label, phase 3, randomised, controlled, non-inferiority trial. Lancet, 399: 1607-1617, 2022.
8) Yoshino I , Moriya Y , Suzuki K , et al.: Long-term outcome of patients with peripheral ground-glass opacity-dominant lung cancer after sublobar resections. J Thorac Cardiovasc Surg, 166: 1222-1231, 2023.
9) Aokage K , Suzuki K , Saji H , et al.: Segmentectomy for ground-glass-dominant lung cancer with a tumour diameter of 3 cm or less including ground-glass opacity (JCOG1211):a multicentre, single-arm, confirmatory, phase 3 trial. Lancet Respir Med, 11: 540-549, 2023.
10) Altorki N , Wang X , Kozono D , et al.: Lobar or Sublobar Resection for Peripheral Stage IA Non-Small-Cell Lung Cancer. N Engl J Med, 388: 489-498, 2023.
11) Mimae T , Okada M : Asian Perspective on Lung Cancer Screening. Thorac Surg Clin, 33: 385-400, 2023.
12) Mimae T , Miyata Y , Tsubokawa N , et al.: Omitting lymph node dissection for small ground glass opacity-dominant tumors. Ann Thorac Surg, Online ahead of print, 2024.
13) Committee for Scientific Affairs, The Japanese Association for Thoracic Surgery, Yoshimura N , Sato Y , et al.: Thoracic and cardiovascular surgeries in Japan during 2021 :Annual report by the Japanese Association for Thoracic Surgery. Gen Thorac Cardiovasc Surg, 72: 254-291, 2024.
14) Mimae T , Saji H , Nakamura H , et al.:Survival of Octogenarians with Early-Stage Non-small Cell Lung Cancer is Comparable Between Wedge Resection and Lobectomy/Segmentectomy: JACS1303. Ann Surg Oncol, 28: 7219-7227, 2021.
15) Mimae T , Miyata Y , Tsutani Y , et al.: Wedge resection as an alternative treatment for octogenarian and older patients with early-stage non-small-cell lung cancer. Jpn J Clin Oncol, 50: 1051-1057, 2020.
16) Mimae T , Miyata Y , Kumada T , et al.: Interstitial pneumonia and advanced age negatively influence postoperative pulmonary function. Interact Cardiovasc Thorac Surg, 34: 753-759, 2022.
17) Mimae T , Miyata Y , Yoshimura K , et al.: Risk of death due to other causes is lower among octogenarians with non-small cell lung cancer after wedge resection than lobectomy/segmentectomy. Jpn J Clin Oncol, 51: 1561-1569, 2021.
18) Mimae T , Wakabayashi M , Sano Y , et al.: Anatomical segmentectomy versus wedge resection for small (≤2 cm) peripheral non-small cell lung cancer in 80 or more aged elderly patients:a randomized phaseⅢ study (JCOG2109, AWESOME). Jpn J Clin Oncol, 53: 1077–1081, 2023.
19) Mimae T , Saji H , Nakamura H , et al.: Sublobar Resection for Non-Small Cell Lung Cancer in Octogenarians:A Prospective, Multicenter Study. Ann Thorac Surg, 116: 543-551, 2023.
20) Mimae T , Miyata Y , Tsubokawa N , et al.: Sublobar Resection in Early Non-Small Cell Lung Cancer With Epidermal Growth Factor Receptor Mutant. Ann Thorac Surg, Online ahead of print, 2024.
21) Okada M , Nishio W , Sakamoto T , et al.: Sleeve segmentectomy for non-small cell lung carcinoma. J Thorac Cardiovasc Surg, 128: 420-424, 2004.
22) Mimae T , Miyata Y , Kumada T , et al.: The intersegmental pulmonary vein is not always located on the intersegmental plane of the lung:Evaluation with 3-dimensional volume-rendering image reconstruction. JTCVS Tech, 16: 132-138, 2022.
PDFを閲覧するためには Adobe Reader が必要です。