日外会誌. 125(2): 146-153, 2024
特集
外科におけるRCT―top journalへの道―
8.小児外科におけるRCT―top journalへの道―
|
広島大学 自然科学研究支援開発センター 檜山 英三 |
ランダム化試験(RCT)は,様々な臨床の診断や治療法の有用性を示すためのゴールドスタンダードであるが,小児外科領域での RCT の報告は数えるほどしかない.RCT を困難にしていることは,多くの人材と労力が必要なこと,疾患自体の発症数が限られることと,標準治療自体が確立していない場合が多いこと,標準治療があっても治療成績が明らかな標準治療を対象として比較を行うため新規治療に過度の期待をすることで振り分けに同意しないことなどがあげられる.特に小児であることから,新規治療の効果を期待した単群での検討を選択することが多いこと自体がtop journalへの道を閉ざしている.小児領域では,悪性腫瘍に関しては RCT が早くから受け入れられ,希少疾患でもあることから国際共同試験の形で,RCT に取り組んだ経緯を本稿で示した.確実なエビデンスを得るためにはRCT が必要であることを理解をすると共に,十分な準備の下で適切なデザインで RCT を行うこと,特に症例数が少ない疾患では,日本全国のみならず,国際共同試験を選択することがtop journalへの近道であることに違いはない.
しかし,明らかにしたい Clinical Question に対して正しいアプローチを行うことも重要である.
キーワード
小児疾患, 臨床研究, 希少性, 国際共同研究, 悪性腫瘍
I.はじめに
ランダム化比較試験(Randomized Controlled Trial,RCT)は1940年代に初めて報告され1),RCTは臨床的介入と治療の有効性を評価するためのゴールドスタンダードの研究デザインとされている.これは,原因と結果について真に有効な推論を実証する唯一の研究デザインであるが,小児外科領域の RCT は世界的に見ても施行された例は50例程度であり1)
2),当該領域においても十分に活用されていないことはいうまでもない.
自身も医学部を卒業して外科医として研修し,小児外科を専攻した私が RCT などの必要性について目覚めたのはずっと後のことで,入局当時は,ほとんどが経験則で物事が決められていた.すなわち,治療方針は指導医が定めるものであり,その根拠は経験によるところとそれまでの先達がのべていたいわゆるレーゲルというもので治療法が決定されていた.
それは,いわゆるシングルアームとして症例を追加し,まとめて検討して症例報告や横断研究を行うのが常であった.これでは,新しい治療法がうまれるのはかなり難しい.その後,2000年頃から Evidence based medicine という用語が用いられるようになり,エビデンスのランクがつけられて,RCT などできちんと有意性が認められたものがエビデンスとされ,治療選択をする根拠となるようになった.
このように,小児外科のみならず外科一般においても,こうした RCT が行われることは,一世代前にはあまりなかった.対照的に,小児腫瘍学の研究では臨床において RCT 試験が有用な効果を示し,適切に設計された欧米の大規模な研究は,高いレベルの結果を導き出して,この20年間で様々な悪性腫瘍の予後を改善して来ている3)
~
6).こうした背景から,自身が RCT に取り組むことになったつたない経験とともに小児外科における RCT について概説する.
II.RCT を行う前に
① Clinical Question
まず,臨床研究を行う際には,Clinical Question として何を明らかにしたいかということが重要である.現状では,何に困っているのか,なにが問題なのか,すなわち「Unmet needs」は,何かということである.外科手術の有効性が知りたいのか,術前診断や治療の違いによる治療成績の差なのか,術後管理の差を見たいのか,とにかく,明らかにしたいことをまずは明確にすることである.それらを明らかにするため,何を行わないといけないのかがおのずと明らかになる.
私の経験からいくと,肝芽腫の治療においては,術前,術後の化学療法としてシスプラチンが有効であることは分かったが,その副作用や晩期合併症が問題であり,できれば化学療法を減量したいという Medical needs があった.そうなると「治療成績をそこなわずに,化学療法が減量できるか」ということになり,予後が良好なグループにおいて従来の治療と減量した治療群の比較を行うことが最も有用なエビデンスが得られるという考えに至ったのである.
② 臨床研究
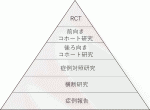
エビデンスレベルという言葉を使ったが,これは臨床研究の結果の信頼性の高さを表している(図1).上位にランダム化比較試験(RCT)があり,以下コホート研究,症例対照研究といった観察研究の順で,RCT こそ信頼できるエビデンスを提供するもので,観察研究からのエビデンスはそれより信頼性が落ちることを意味している.しかし,RCT においても,多くのバイアスや交絡因子がありこれらを確実に処理することが必要となる.通常のコホート研究では,対照群と試験群に分けた際,この 2 群の背景が同一であるか否かが問題となる.また,試験群がより有効であると期待した際の「医師の裁量,患者の希望」などもバイアスとなる.これらは RCT では影響を受けない利点がある.一方,RCT では,これらの背景を同一にするために,選択基準,除外基準を細かく定めるが,そのために適格となる症例数が減少し,結果的に試験が成立しにくくなることがある.また,安全性を確保して治療効果を厳密に評価するために,治療成績をすぐに臨床に応用できないことも問題となる.例えば,安全性を担保することや,臨床情報を正しく評価するために,年齢層で乳児を除いたり,学童に限定するなどを行うと,結果的に疾患全体を示す結果に至らないことも考えられる.これらに十分に配慮して臨床試験の体制を組みたてることが必要となる.
③ 対象症例数
これらを踏まえて,比較をするための対象とすべき症例の群を定めて,適格性のある症例を決定する.次に,実際に臨床研究で比較を行うとするとそれらの症例がどれだけの期間にどの程度発生しているかというデータが必要となる.単一施設で実施するのであれば,その施設での年間の診療実績を調べれば,必要な対象症例がどの程度発生しているかを把握できる.鼠経ヘルニアなどの小児外科でよく診られる疾患であれば,単一施設での実施も可能なのかもしれないが,多くの疾患は各施設での診療数は限られており,多施設共同研究となることが少なくない.その場合は,参加する施設の発生数あるいは必要な症例数から参加施設を決定することになるが,小児外科の場合は,学会登録のデータベ―スや NCD 登録などのデータを用いて,対象となる症例の発生状況をみて,試験の枠組みを決定し,全国規模の多施設共同研究を計画する.また,さらに希少な疾患の場合は,国際共同臨床試験が必要となる.
私が取り組んでいる小児肝腫瘍の研究では,従来はシングルアームでの試験を行っても 10 年近くの期間が必要であり,かつエビデンスを得ることが困難であった7).そのために,以下の④に示した準備をあらかじめ行い,国際共同試験を行うこととした3).
④ 診断基準やリスク分類の統一
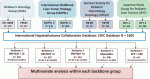
多施設共同試験を行う際には,疾患の診断,重症度判定やリスク分離を統一することがまず必須となる.本邦での小児悪性腫瘍に対する全国多施設共同研究においては,中央病理診断を導入して,診断レベルを均一としてきた.さらに,小児肝腫瘍に対して国際共同試験を行うにあたっては,まずは国際共通の病理診断基準の策定が必要であり,その作業を日米欧の専門家を集めて行った8).次いで,病期分類は,米国では COG (Children’s Oncology Group)分類,欧州では PRETEXT 分類,本邦では日本小児外科学会分類が用いられてきたが,これらを欧州の PRETEXT 分類に統一し,さらに,この分類の付加因子の定義についても定義を再検討して統一した.これらの因子を定めたのちに,過去に行った各グループの臨床試験の経験例を(CHIC: Children’s Hepatic tumor International Consortium)としてデータベース化,約 1,600 例のデータベースを構築した9)(図2).これをもとに,リスク層別因子を決定して,肝芽腫は超低リスク,低リスク,中間リスク,高リスクに分類する国際共同リスク分類を提案した10)(表1).診断基準や適格基準のためのこうした基盤整備を行ったのちにRCTを計画した.
また,RCT を検討するまえに,臨床研究を行うためのノウハウを知ることが必要である.ノウハウとは,小児外科分野での Unmet medical needs としての研究テーマについて,出口となる研究目的を明らかにして,進むべき方法を共有して研究デザインを立てることである.次に,モノ,カネ,ヒトが必要である.モノとなる研究材料があり,カネとなる研究費があり,さらに,研究を支えてくれる共同研究者や統計学者などが必要である.

III.RCTの実施
① 研究計画書(プロトコール)の作成
研究デザインとして重要なのが,研究計画書(研究プロトコール)であり,これには,研究概要,研究目的,研究対象とその数,研究期間,実施方法,インフォームドコンセント(アセント),統計解析を行うエンドポイント,研究組織などが最低限必要な項目となる.症例報告や症例を集めた横断研究にしか慣れていない小児外科医にとっては楽な仕事ではない.プロトコールに必要な内容は表に示す.
研究概要は,専門的な用語はできるだけ避けて平易な文章で分かりやすく作成する.重要なのは統計学的視点からのデザインである.これは,統計家に意見を聞くか,統計家に対象数などの設定を任せることは必須である.統計学的には,バイアスがないことを前提に方法論が構築されるが,多くの研究にはバイアスが存在することが多い.バラツキを少なくするためにはサンプル数を増やすことで回避されるが,偏りによるバイアスは数では解消できないため,それを解消する最大の方法がランダム化であり,盲検化は対象者に対する医師の評価やデータ管理へのバイアスを避ける最も良い方法である.
研究計画書の書き方については,多くの論文などがあり,これを参考にされたい11).あらかじめ RCT を設定して,バイアスを最小限にしたデータ取得を行う体制で臨床試験を行うが,ここで重要なのは,エンドポイントを正しく定めておくことである.臨床研究/臨床試験におけるエンドポントは,“Outcome measure”(結果を測るものさし)の意味で用いられる.主要評価項目,副次評価項目,探索的評価項目に分けて定め,物差しであるから,評価など抽象的なものでなく,測定できるものを掲げる.試験の途中や試験後に新たな評価項目を追加したり,変更することは原則として認められない.ここをないがしろにすると,質の良い臨床試験とは評価されず,いわゆる top journal への道は閉ざされることになる.
② 実施体制の構築
臨床試験を実施する際は,治験や臨床研究においては,それぞれの倫理指針に則った体制を構築して,審査を経たのちに実施することは言うまでもない.これは,あくまで手続きであり,実際の RCT などの臨床研究の実施においては,統計家をはじめ,多くの関連した専門職を配置する.われわれが取り組んでいる国際共同試験においては(表2),参加する団体からそれぞれ統計家が参加して試験のデザインを決定した.さらに,放射線診断,薬剤投与,手術療法などは各領域の専門家によるガイドライン作成などを行い,RCTからなる試験を組み立てた.
モニタリングや監査は,臨床試験の科学的な質とデータの信頼性を確保する手段であり,治験では GCP(Good Clinical Practice) に則りこれまでも実施されているが,臨床研究においてもこれらを取り入れることが必要である.これらの試験は,ICH GCP R2 に準拠して行われることが必要であり,研究結果の信頼性の確保に重点をおいて実施する.これらの管理は,試験の中途でも いわゆるPDCA サイクルにて検討し,変更も可能で,Quality management system として現在導入されている.モニタリングの手法も研究の性質などによって適切に効率的行うことが許されている.すなわち,被験者保護と試験結果の信頼性担保の重要視して効率的に行う.その手順書を示すことも重要である.すなわち,エラー率についてどの程度許容できるかをリスクアセスメントの時期に明らかにして,これらを適切に扱い正しい結果を得る.リスク管理もある程度軽減しながら運用してその評価を行うことになる.重要なプロセスとして,被験者保護,評価項目,有害事象があげられる.これらのリスクを管理することである.
③ 結果の報告
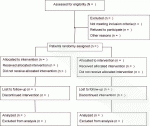
あらかじめ設定された評価項目について,正しい統計学的解析を行うことが必須である.そのためには,図3のような CONSORT diagram を作成して,その図に従って,解析を行っていく.その際は,P値は,<.05 や<.01 ではなく両側のP値を二桁までで記載すること,必要に応じて,絶対差と相対差の両方と信頼区間を含む結果を報告する.
治療成績や予後に強く関連するエビデンスが RCT で得られれば,ハイインパクトとして評価され,結果的にそれなりの雑誌に掲載されることとなる.雑誌によっては,RCTでの投稿のガイドラインが示されていて,これに沿って論文を作成することがアクセプトには近道である.もちろん,臨床研究をあらかじめ登録した情報,プロトコールやファンディングに関しても掲載が必須となる.

IV.小児外科におけるRCTの現状と課題
小児外科領域は,胎児手術から,新生児疾患,肝胆道系疾患,直腸肛門奇形,炎症性疾患,泌尿器疾患,ヘルニアなどの体表疾患,悪性腫瘍など多岐にわたる.臨床研究は様々なアプローチがなされているが,小児であることや疾患の希少性から,RCT が行えない疾患も少なくない.これまでに行われた RCT としては,胎児横隔膜ヘルニアに対する胎児鏡下気管閉塞術(FETO:fetoscopic endoluminal tracheal occlusion)の RCT や12),胆道閉鎖症術後のステロイド投与の有効性に対する RCT が行われている13)
14)が,結果的に評価の高いジャーナルでの発表に至っているとは必ずしも言えない.その原因は,これらの疾患は,重症度や背景がかなり異なっている症例の集まりであり,RCTを行った成果が科学的に正しく評価されるためには,それなりの症例数が必要となるのであるが,疾患そのものの症例数に限りがあるがために,有意性が導けなかったと推察する.このように,RCT を行えば必ずレベルの高いエビデンスが得られるわけではないので,RCT を計画する際は,十分な準備とともに症例の集積についての実現性を担保しておくことが望ましい.しかし,現実には,RCT を行えることの方が少なく,単一のコホート研究や観察研究を行う疾患の方が圧倒的に多い.現在は,小児外科が取り扱う悪性腫瘍の中でも,私共が取り組んでいる小児肝腫瘍に対する国際共同臨床試験では,国際共通の病理,病期,リスク分類を準備したのちに,いくつかの具体的な Clinical Question に応じたリスク別の RCT を策定して運用している.グローバル研究は,疾患の希少性についての問題を解決できる一方で,試験内容のクオリティやモニタリングについては細心の注意が必要である.本邦の小児・AYA(Adolescent and Young Adult) 世代の胚細胞腫瘍は,米国の小児と成人の臨床試験のグループ COG と NRG が行っている臨床試験に参加する形で RCT を行い,標準リスクでのシスプラチンをカルボプラチンに変更して,内耳障害などの晩期合併症軽減を目的とした試験を行っている13)
14).また,神経芽腫においては,RCT ではないが,高リスク群では全国多施設共同前向き臨床試験が行われ,低・中間リスクでは治療軽減を目的の観察研究が行われ,乳児の低リスク患者では無治療経過観察が安全に行いえるかについて前方視的な臨床試験が行われている13)
14).腎腫瘍に対しては,グローバル研究であるが観察研究である UMBRELLA プロトコールにそって,多種にわたる小児腎腫瘍に対する試験が行われている5).
こうした RCT 以外でも,後向き観察研究といえども臨床研究を正しく客観的に施行することで,その成果が公表され,評価されることも少なくない.本稿の内容とは少し離れるが,かつて筆者は,1984 年から約 20 年間日本が世界に先んじて行った厚生労働省の母子保健課の事業として行われた神経芽腫検査事業,いわゆる神経芽腫マススクリーニング事業の解析にかかわった.この事業は RCT として計画されなかったことが後々の批判や休止につながった最大の原因であり,欧米の小規模な RCT の結果で神経芽腫の死亡率の低下が認められなかったという報告を受けて,先行した大規模研究であったにもかかわらず,2003 年に休止に追い込まれた.この結果は RCT の重要性を示すとともに,多くの統計学者から批判されたことは事実であるが,彼らがこの事業への酷評を行いながら,正しい臨床研究の在り方を示さなかったことには大きな疑問を投げかけざるを得ない.実際には,2,000 万人を超える乳児が受診した事業であり,本邦からこの結果の集計を行い開示することは,国家事業としての責務であり,その頃筆者は日本小児外科学会の悪性腫瘍委員会に属していたことから,後ろ向き研究を行った.結果として,スクリーニングを受けた群の発症率は 2.8 倍となり,明らかに過剰診断の症例が含まれていたものの,進行例が減少し,死亡症例の調査も合わせると神経芽腫による年間死亡率がスクリーニング受診例では半減していた事が明らかとなった.この事実は,Lancet の Editorial Board に受け入れられ,同誌への掲載に至っている15).RCT はtop journalへの掲載を目指したレベルの高いエビデンスを得るためにぜひ取り組むべき研究手段であるが,一方で,明らかにしたい Clinical Question が何であるかも,重要である.
V.おわりに
top journalへの道として,小児外科領域での RCT のつたない経験について論説した.top journalへの掲載が最終目的ではなく,いかに臨床に有用な質の高いエビデンスを得て小児外科診療を発展させるかが重要なのであって,そうした結果を報告し,世界中から評価された論文が,いずれ多くの引用とともに後世に残ることでその掲載雑誌がtop journalになっていく.本稿が小児外科に携わる研究者にとって,科学性と被験者の安全性が担保された研究を押し進めていただく一助となれば幸いである.
利益相反:なし
文献
1) Scowen EF , Garrod LP :The streptomycin-sulphadiazine treatment of undulant fever. Br Med J, 2: 1099-1101, 1948.
2) Curry JI , Reeves B , Stringer MD :Randomized controlled trials in pediatric surgery: could we do better? J Pediatr Surg, 38: 556-559, 2003.
3) 檜山 英三 , 兒島 正人 , 栗原 将 ,他 :【小児外科臨床研究の基本と展望】国際共同臨床試験.小児外科,52: 710-714,2020.
4) 田尻 達郎 , 文野 誠久 :【小児外科臨床研究の基本と展望】小児悪性固形腫瘍の臨床研究の現状と今後.小児外科,52: 763-767,2020.
5) 大植 孝治 :小児がんの国際共同臨床試験の現状と課題 小児腎腫瘍の国際共同試験の現状と今後. 日小児血がん会誌,57: 92-95,2020.
6) 小野 滋 , 黒田 達夫 :小児がんの国際共同臨床試験の現状と課題 胚細胞腫瘍における国際共同臨床試験(AGCT1531).日小児血がん会誌,57: 210-214,2020.
7) Hiyama E , Hishiki T , Watanabe K , et al.:Outcome and Late Complications of Hepatoblastomas Treated Using the Japanese Study Group for Pediatric Liver Tumor 2 Protocol. J Clin Oncol, 38: 2488-2498, 2020.
8) López-Terrada D , Alaggio R , de Dávila MT , et al.:Towards an international pediatric liver tumor consensus classification: proceedings of the Los Angeles COG liver tumors symposium. Mod Pathol, 27: 472-491, 2014.
9) Czauderna P , Haeberle B , Hiyama E , et al.:The Children’s Hepatic tumors International Collaboration (CHIC): Novel global rare tumor database yields new prognostic factors in hepatoblastoma and becomes a research model. Eur J Cancer, 52: 92-101, 2016.
10) Meyers RL , Maibach R , Hiyama E , et al.:Risk-stratified staging in paediatric hepatoblastoma: a unified analysis from the Children’s Hepatic tumors International Collaboration. Lancet Oncol, 18: 122-131, 2017.
11) 福田 治彦 :【小児外科臨床研究の基本と展望】研究の構想とデザイン.小児外科,52: 661-669,2020.
12) Wada S , Ozawa K , Sugibayashi R , et al.:Feasibility and outcomes of fetoscopic endoluminal tracheal occlusion for severe congenital diaphragmatic hernia: A Japanese experience. J Obstet Gynaecol Res, 46: 2598-2604, 2020.
13) Lu X , Jiang J , Shen Z , et al.:Effect of Adjuvant Steroid Therapy in type 3 Biliary Atresia: A SingleCenter, Open-Label, Randomized Controlled Trial. Ann Surg, 277: e1200-e1207, 2023.
14) Alonso EM , Ye W , Hawthorne K , et al.:Impact of Steroid Therapy on Early Growth in Infants with Biliary Atresia: The Multicenter Steroids in Biliary Atresia Randomized Trial. J pediatr, 202: 179-185. e4, 2018.
15) Hiyama E , Iehara T , Sugimoto T , et al.:Effectiveness of screening for neuroblastoma at 6 months of age: a retrospective population-based cohort study. Lancet, 371(9619): 1173-1180, 2008.
PDFを閲覧するためには Adobe Reader が必要です。