日外会誌. 124(3): 284-288, 2023
会員のための企画
重症心不全に対する骨格筋筋芽細胞シート移植療法開発における産官学連携
|
大阪大学 心臓血管外科 宮川 繁 |
これまで,当科においては,心不全に対する自己筋芽細胞シート“ハートシート”,他家iPS細胞由来心筋細胞シートの開発を行ってきた.前者は,東京女子医科大学との共同研究にて基礎研究を行うと同時に,テルモ株式会社(以下,テルモ社)は臨床に用いることのできる筋芽細胞の単離に関する方法論を取得し,開発段階から“産”と“学”が共同で開発を行ってきた.また,同時期には,再生医療等製品に関する早期承認制度が制定され,その波に乗り,本製品は早期承認されることとなった.また,iPS細胞由来心筋細胞シートは,これまでの経験を生かした産官学連携により,現在,医師主導型治験の段階にある.現在,再生医療等製品開発において,産官学連携が盛んに行われており,本邦における新しい産業の一つになろうとしている.
キーワード
細胞移植, 重症心不全, 骨格筋筋芽細胞シート, iPS細胞由来心筋細胞シート, 産官学連携
I.はじめに
外科領域にて医療機器や再生医療等製品開発は,手術手技を熟練化するのと同様,手術成績向上のためには必須である.その中で“学”のみで基礎研究を行っても,臨床応用への出口を探ることは困難であり,実用化は容易ではない.一方で,“産”は製品化等の技術にはたけているが,医療におけるニーズの把握,科学的なメカニズム解明には門外漢である.この“学”と“産”が強力にタッグを組むことにより,新しい医療機器,再生医療等製品が生まれ,その上で,“官”による制度設計,レギュレーション,開発費用投入が加わることにより,一層製品開発に拍車がかかる.本稿では,ハートシートの開発の歴史を述べるとともに,開発を通して行ってきた産官学連携の歴史そしてあり方について概説する.
II.自己骨格筋筋芽細胞シートおよびiPS細胞由来心筋細胞シート開発における産官学連携の歴史
開発を開始した2000年当初,脳死法案化の心臓移植が再開されたものの,ドナーは極めて不足していた.当時,体外式人工心臓を装着した心不全患者は,長期入院を強いられる状況であり,ドナーを待ちながら,入院中に感染,脳出血等の合併症により亡くなられる患者が相次いでいた.その状況の中で,心移植,人工心臓を支えうる新しい治療を模索する気運が生まれ,開発されたのが細胞シート治療である.本治療方法は東京女子医科大学の岡野光夫先生,清水達也先生が開発され1),大阪大学で実用化された.開発当初は,ラット新生仔の心臓から単離された心筋細胞を,温度応答性培養皿を用いてラット由来心筋細胞シートを作成し2),その有効性に関して非臨床研究を行っていた3).一方で,臨床の現場では,病棟には体外式人工心臓を装着した患者であふれ,この状況を一刻も早く打開する必要性に迫られていた.しかし,ラット新生仔の心筋細胞を移植することは臨床の現場では容易ではなく,より迅速に臨床応用するためにラット新生仔心筋細胞から患者本人の骨格筋筋芽細胞に変更した.大阪大学では様々な心不全モデル動物を用いて骨格筋筋芽細胞シートの有効性,安全性を検証した(図1)4)
~
8).
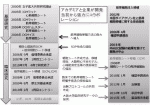
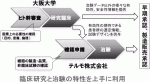
一方で,テルモ社は,心不全領域における細胞治療の可能性をいち早く認知し,米国ダイアクリン社から筋芽細胞の単離方法の権利を獲得し,心不全に対する筋芽細胞の心筋内注射の治験を計画していた.当時,フランスのメナシェ教授が,虚血性心筋症に対して,自己筋芽細胞を心筋に注射器を用いて移植したが,心機能の改善を認めず,致死性不整脈が起こるという結果を発表した9).そのため,テルモ社は自己筋芽細胞の移植に関して否定的な見解を抱いていた.しかし,当科で行ってきた筋芽細胞シートの有効性に関する非臨床研究データをテルモ社に全て開示すると同時に,テルモ社に心不全動物の作製方法,心臓超音波の測定方法等非臨床研究の方法論を伝授し,テルモ社は本治療法の有効性に関する可能性を実感するに至った.この時点で,大阪大学とテルモ社の今後の製品化に関する方向性が意思統一され,どちらにとってもWin-Winの関係を築き,再生医療における産学連携体制が構築された.両者における産学連携に関する歩みを図に示す(図2).また,大阪大学では,体外式人工心臓を装着した拡張型心筋症患者に対して,自己筋芽細胞シートを移植する臨床研究を開始し,4例のうち2例に心機能の改善を認め,その2例が人工心臓から離脱が可能であった10).当時,病棟に体外式人工心臓を装着した心不全患者が多数おられ,こういった新しい治療を行うことでBridge to Recoveryが可能であることを示した.また,臨床研究において,全ての薬物治療や外科的治療が終了している虚血性心筋症患者に本治療を行い,安全性を確認すると同時に,本治療に対するResponderとNon-Responderが存在することを示した11).これらの臨床研究のデータをテルモ社に対して開示し,テルモ社は本データに基づいて,企業治験の計画を立案,実施し,最終的に,保険収載を得ることが可能となった(図3)12).細胞の安全性の検証,人体に移植できる細胞単離法,臨床研究から治験にいかにしてつなげていくか等々“学”がもっていない面を“産”が補いつつ,一方で“産”がもっていない科学的,医学的な側面を“学”が補いつつ,お互いの弱点を克服できるように綿密に協力した産学連携であったと考えている.現在では市販後調査の段階であり,東京大学,東京女子医科大学,東京医科歯科大学,順天堂大学,新潟大学,名古屋大学,東北大学,九州大学,福島医科大学,北海道大学で本治療が行われている.上記のように,最終の有効性,安全性が検証されている状況であり,“学”の中では,現在の心不全治療の変革を求めて多数の先生方が参集され,新しい治療法の検証が行われている.
また,“官”においては,当時,欧米と比較して医療機器開発等の遅れを実感し,日本が主導できる分野は何なのか,そして新しい制度,産業の構築はできないかの議論が行われていた.その議論の中で,再生医療等製品に関する早期承認制度が策定された(図4).本制度は世界に先駆けて本邦で制定されたが,単群試験にて保険収載することに対する批判が持ち上がった13).しかし,その後欧米において同様の制度が発足し,現在では日本より欧米のほうが多くの再生医療等製品が上市されている14).加えて,同時期に山中教授のノーベル医学賞受賞も相まって,本邦においては,再生医療に関するグラントが多数発出され,“官”における再生医療に対する気運は高まりをみせていた.
上記のように,再生医療は,“学”と“産”が開発の段階から,お互いの強み,弱点を把握し,共同関係を築きながら,開発されてきた.さらに,“官”においては,新しい産業を切望する気運やそれを後押しする制度設計の模索が始まり,これらが同じベクトルを持つことによって強固な産学官連携が形成された.
現在,再生医療等製品の開発において,このハートシートにおける産官学連携を一つの例として,各施設にて製品開発が行われている.


III.心臓血管外科における産官学連携の在り方
ハートシートは,上記のように,開発の段階から“学”と“産”が,お互いの強み,弱点を把握し,共同関係を築きながら,開発されてきた.そして時代の流れに呼応し,“官”が時期を逸さず,世界に先駆けて制度設計を行った賜物であると考えている.
前述したとおり,外科の発展には,外科技術を支える医療機器,再生医療等製品の開発が必須であり,“学”“産”“官”の3者が,独りよがりのニーズを叫ぶのではなく,共同して,同じ方向性に向かって連携を組むことが必要であり,それぞれの特性を分かりあいながら協調することが必要であると考えている.例えば,“学”においては,“産”は何を欲しているのか?“官”は国政としてどの方向性を模索しているのかをしっかり把握しながら,そして医療現場におけるニーズは何であるのかを絶えず問いかけながら,効果的な産官学連携を進めていく必要がある.
IV.おわりに
今後の外科領域において,われわれが経験した産官学連携を土台として,医療機器,再生医療等製品の開発が進み,本邦の外科学がさらに発展すると同時に,世界に冠たる製品が誕生することを願ってやまない.
利益相反
講演料など:テルモ株式会社
寄付講座:テルモ株式会社
文献
1) Okano T, Yamada N, Sakai H, et al.: A novel recovery system for cultured cells using plasma-treated polystyrene dishes grafted with poly(N-isopropylacrylamide). J Biomed Mater Res, 27: 1243-1251, 1993.
2) Shimizu T, Yamato M, Isoi Y, et al.: Fabrication of pulsatile cardiac tissue grafts using a novel 3-dimensional cell sheet manipulation technique and temperature-responsive cell culture surfaces. Circ Res, 90:e40, 2002.
3) )Miyagawa S, Sawa Y, Sakakida S, et al.: Tissue cardiomyoplasty using bioengineered contractile cardiomyocyte sheets to repair damaged myocardium:their integration with recipient myocardium. Transplantation, 80: 1586-1595, 2005.
4) Memon IA, Sawa Y, Fukushima N, et al.: Repair of impaired myocardium by means of implantation of engineered autologous myoblast sheets. J Thorac Cardiovasc Surg, 130: 1333-1341, 2005.
5) Hata H, Matsumiya G, Miyagawa S, et al.: Grafted skeletal myoblast sheets attenuate myocardial remodeling in pacing-induced canine heart failure model. J Thorac Cardiovasc Surg, 132: 918-924, 2006.
6) Kondoh H, Sawa Y, Miyagawa S, et al.: Longer preservation of cardiac performance by sheet-shaped myoblast implantation in dilated cardiomyopathic hamsters. Cardiovasc Res, 69: 466-475, 2006.
7) Sekiya N, Matsumiya G, Miyagawa S, et al.: Layered implantation of myoblast sheets attenuates adverse cardiac remodeling of the infarcted heart. J Thorac Cardiovasc Surg, 138: 985-993, 2009.
8) Miyagawa S, Saito A, Sakaguchi T, et al.: Impaired myocardium regeneration with skeletal cell sheets--a preclinical trial for tissue-engineered regeneration therapy. Transplantation, 90: 364-372, 2010.
9) Menasche P, Alfieri O, Janssens S, et al.: The Myoblast Autologous Grafting in Ischemic Cardiomyopathy (MAGIC) trial: first randomized placebo-controlled study of myoblast transplantation. Circulation, 117: 1189-1200, 2008.
10) Yoshikawa Y, Miyagawa S, Toda K, et al.: Myocardial regenerative therapy using a scaffold-free skeletal-muscle-derived cell sheet in patients with dilated cardiomyopathy even under a left ventricular assist device:a safety and feasibility study. Surg Today, 48: 200-210, 2018.
11) Kainuma S, Miyagawa S, Toda K, et al.: Long-term outcomes of autologous skeletal myoblast cell-sheet transplantation for end-stage ischemic cardiomyopathy. Mol Ther, 29: 1425-1438, 2021.
12) Sawa Y, Yoshikawa Y, Toda K, et al.: Safety and Efficacy of Autologous Skeletal Myoblast Sheets (TCD-51073) for the Treatment of Severe Chronic Heart Failure Due to Ischemic Heart Disease. Circ J, 79: 991-999, 2015.
13) Stem the tide. Nature, 528: 163-164, 2015.
14) 吉田 昌生:日米欧の新薬承認状況と審査期間の比較- COVID-19ワクチンの事例も踏まえた日本の課題-.政策研ニュース,64,2021.
PDFを閲覧するためには Adobe Reader が必要です。