日外会誌. 122(2): 166-171, 2021
特集
肝胆膵領域腫瘍におけるBorderline resectable/Marginally resectableとは
―術前治療の可能性について―
6.胆嚢癌
|
1) 名古屋大学大学院医学部 医学系研究科腫瘍外科 水野 隆史1) , 江畑 智希1) , 梛野 正人1)2) |
胆嚢癌は疾患特異的な自覚症状に乏しく,初診時に高度のリンパ節転移や隣接他臓器浸潤を認める進行癌として発見される症例も少なくない.拡大切除術式の積極的適応により進行胆嚢癌の切除率は向上したが,拡大切除によっても非根治的切除となる症例や切除後の早期再発症例も存在し,治療成績は未だ満足できるものではない.近年,切除不能胆道癌に対する薬物療法の治療成績が急速に進歩している一方,局所進行癌における切除可能/切除不能の境界については施設間で異なっており明確なコンセンサスが得られていない.しかしながら切除可能/不能を明確に判断しうる症例の間には,技術的に切除が可能であっても非根治切除となる蓋然性が高く,予後延長効果が期待しづらい症例群が存在し,かかる症例群を“borderline resectable”胆嚢癌として独立して定義することにより,集学的治療戦略の有効性を議論できる可能性がある.
キーワード
胆嚢癌, 肝膵十二指腸切除, hepatopancreatoduodenectomy
I.はじめに
胆嚢癌は疾患特異的な自覚症状に乏しく,初診時に高度のリンパ節転移や隣接他臓器浸潤を認める進行癌として発見される症例が少なくない.外科切除は胆嚢癌において唯一根治が望みうる治療であり,過去の治療開発においては局所進行症例に対する拡大切除術式の積極的適応が切除率を向上し,かかる拡大切除術式の手術成績の向上が生存成績の向上に大きく関連してきた1)
2).2010年に報告された切除不能進行再発胆道癌に対する第3相ランダム化比較試験の結果によりgemcitabine + cisplatin療法が切除不能胆道癌に対する一次標準治療として確立し3),本報告以降,本邦からも複数のランダム化比較試験の結果が相次いで報告され4)
5),切除不能胆道癌に対する薬物療法の治療成績は近年急速に向上している.
一方,胆嚢癌治療のgold-standardである外科切除において,局所進行症例における “切除可能/不能”の境界は明確となっておらず,局所進行症例に対する拡大切除術式の適応度も施設間で異なっている.
現在,膵癌において,根治切除が可能であり有意な生命予後延長効果が期待しうる“切除可能症例”と,適応しうる最大限の拡大切除術式を適応しても根治切除不可能な“切除不能症例”の間に存在する症例群を“切除可能境界(borderline-resectable)症例”として定義し,集学的な治療戦略を用いてかかる症例群に対する治療成績を向上させることが試みられている.局所進行における切除可能/不能の境界が未だ定まらない胆嚢癌においてもこの概念を適応することにより,切除可能/切除不能症例に対する治療戦略とは異なる,新たな集学的治療戦略が確立できる可能性がある.本稿では局所進行胆嚢癌に対する著者の施設における拡大切除術式の成績を示し,“切除可能境界(borderline-resectable)胆嚢癌”という概念が設定可能かについて考察したい.
II.胆嚢癌の“外科的”切除可能/切除不能境界
現行の胆道癌診療ガイドライン(第3版)では,切除不能胆道癌について,「遠隔転移を伴う胆道癌は切除不能と考えられる.局所進展による切除不能因子については明らかなコンセンサスは得られていない」と述べられており6),進行胆嚢癌に対する拡大切除が積極的に行われ,治療成績についての多数の報告が存在する本邦においても,局所進行による切除可能/不能の境界や切除不能因子について明確なコンセンサスが得られていない現状を表している.これまでに報告された切除不能進行胆道癌に対するランダム化比較試験においても,局所進行切除不能の定義についての明確な記載は認められず,切除可能/不能の判断は試験参加施設での判断に任されている可能性が伺える.しかしながら技術的な観点において,1)胆嚢周囲臓器(肝・肝外胆管・膵頭十二指腸部・結腸)の合併切除を行っても根治切除不可能,2)再建不可能な脈管(肝動脈・門脈・肝静脈)浸潤を認める,3)広範囲肝切除が必要であるが十分な残肝機能の温存が不可能な症例は,根治切除は不可能であるため,少なくともこれら三条件を局所進展による切除不能因子と考えることに異論はないと思われる.
一方,技術的に切除可能と判断される癌においても,癌の進展様式に応じて多様な切除術式が適応されるため,切除可能胆嚢癌に対するいわゆる“標準”切除術式というものは存在しない.しかしながら,胆嚢漿膜下層あるいは胆嚢床部筋層周囲結合織までにとどまる胆嚢癌に対する限局肝切除(胆嚢床切除)+領域リンパ節郭清は国内外の施設で広く適応されており,本術式により切除可能な胆嚢癌を“切除可能”胆嚢癌として定義することについてもまた異論はないと思われる.
上述した,明らかな“切除可能”症例と“切除不能”症例の間には,限局肝切除+領域リンパ節郭清により切除される範囲を超え進展・浸潤するものの,拡大切除術式の適応により,根治切除が可能となる症例群が存在し,癌の進展範囲に応じて,1)広範囲肝直接浸潤・肝門部浸潤例に対する肝切除(+肝外胆管切除),2)膵頭十二指腸部浸潤例に対する限局肝切除+膵頭十二指腸切除(minor HPD)(図1a),3)胃・結腸浸潤例に対する隣接臓器合併切除を伴う切除といった拡大切除術式が適応される.さらに,高度な肝直接浸潤・肝門部浸潤と膵頭十二指腸部浸潤の両者を認める高度進行胆嚢癌に対し,本邦の一部の専門施設を中心に広範囲肝切除兼膵頭十二指腸切除(Major HPD)(図1b)が適応されてきた7)
~
9).

III.進行胆道癌に対する拡大切除術式の成績
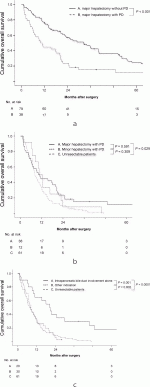
著者らは進行胆嚢癌に対する拡大切除術式,特に肝切除兼膵十二指腸切除(HPD: hepatopancreatoduodenectomy)の意義を検討するため,1996年~2016年の20年間に自施設で施行した広範囲肝切除兼膵頭十二指腸切除(Major HPD)例(n=38)と広範囲肝切除例(n=79)を比較した10).広範囲肝切除例に比しMajor HPD例では,Clavien-Dindo分類Grade 3以上の術後合併症率(87% vs. 58%,P=0.002),周術期死亡率(18% vs. 5%,P=0.037)が高く,術後全生存(中央値, 10カ月 vs. 32カ月,P<0.001)は不良であった(図2a).またMajor HPD施行例の約1/3の症例に組織学的大動脈周囲リンパ節転移が存在していた.
また,同時期に行った限局肝切除+膵頭十二指腸切除(minor HPD)例(n=12)とMajor HPD例の比較では11),minor HPD例に比しMajor HPD例ではISGLS-Grade B以上の術後肝不全発生率(25% vs. 68%, P=0.017)が高率であったが,Clavien-Dindo分類Grade 3以上の術後合併症率(92% vs. 87%, P=1.00),術後全生存(中央値,10カ月 vs. 11カ月,P=0.591)はほぼ同等であった(図2b).膵頭十二指腸切除を併施した要因別に生存成績を検討すると,その要因が腫瘍の膵頭十二指腸部直接浸潤または膵頭部リンパ節転移であった症例は経胆嚢管的膵内胆管進展のみが要因であった症例に比し,術後全生存(中央値:7.5カ月vs. 20.4カ月,P=0.001)が不良であった(図2c).
以上の自施設での結果をまとめると,広範囲肝直接浸潤・肝門部浸潤例に対する広範囲肝切除や経胆嚢管的膵内胆管進展症例に対するHPDは拡大切除術式の適応により良好な予後が期待できる一方,膵頭部直接浸潤・膵頭部周囲リンパ節転移を認める症例に対するHPDの切除後の生存成績は不良であり,拡大切除術式が適応される取り扱い規約上のclinical T3/T4症例群の中でも切除後の予後に差がある事が認められた.
IV.切除不能胆嚢癌に対する化学療法とBorderline resectable/marginally resectableの概念
切除不能進行胆道癌に対するgemcitabine + cisplatin療法の有効性を検討したランダム化第三相試験(ABC-02)以降,複数の前向き試験の結果が報告されており,各々の臨床試験における試験治療群の全生存は11カ月~19カ月,奏効率は26%~45%と薬物療法の開発が近年急速に進んでいることが伺われる4)
5)
12).また,全身化学療法の奏功が得られた初回切除不能胆道癌症例に対し外科切除を行う,いわゆるconversion surgeryの報告が少数例での検討ではあるものの報告されており13)
14),化学療法と外科切除による集学的治療効果による予後延長効果が期待できる症例が一定程度存在することが示唆されている.
現在,膵癌において,腫瘍が門脈や上腸間膜動脈など主要血管に浸潤を認め,手術先行による外科的切除を施行しても高率に癌が遺残し生存期間延長効果を得ることができない可能性がある癌を切除可能境界膵癌(borderline resectable pancreatic cancer)として定義し,術前化学療法または化学放射線療法の奏効により腫瘍の完全切除率を高め,長期生存が期待しうる症例を効果的に選択する治療戦略の開発が進んでいる.Katzら15)
16)は,切除可能境界(borderline resectable)に合致する症例は,1)術式の拡大により周術期合併症のリスク上昇が懸念され,2)技術的に切除可能であるも非根治的切除になる蓋然性が高く,3)切除後の早期再発により生命予後延長効果が乏しい症例群であると述べている.局所進行胆嚢癌症例において,この“Borderline resectable”の概念に合致する症例群を,著者の施設における成績をもとに敢えて設定するとすれば,腫瘍の膵頭十二指腸部直接浸潤や膵頭部リンパ節転移を有しHPDが適応となる症例群は技術的に切除可能であるものの,“標準的”切除術式である限局肝切除+領域リンパ節郭清に比し周術期合併症のリスクや非根治的切除となる蓋然性が高く,切除後の生命予後延長効果が乏しいため,この定義に当てはまる症例群といえる.
V.おわりに
胆嚢癌においてborderline resectableの概念が設定可能か否か,またどのような症例をborderline resectableとして定義するかについて,今後も多くの議論が必要であることは言うまでもない.しかしながら画像的・外科的に明確に切除可能/不能を定義しえない症例群を一つの独立したカテゴリとして設定することは,局所進行胆嚢癌に対する集学的治療戦略を促進するうえで重要であり,また強力な薬物療法regimenの開発によりかかる集学的治療戦略の重要性は増してゆくと思われるため,胆嚢癌治療をリードしてきた本邦においてBorderline resectable GBCの概念を確立するための意見集約が進むことを期待したい.
利益相反:なし
文献
1) Kondo S , Nimura Y , Hayakawa N , et al.: Extensive surgery for carcinoma of the gallbladder. Br J Surg, 89(2): 179-184, 2002.
2) Nishio H , Ebata T , Yokoyama Y , et al.: Gallbladder cancer involving the extrahepatic bile duct is worthy of resection. Ann Surg, 253(5): 953-960, 2011.
3) Valle J , Wasan H , Palmer DH , et al.: Cisplatin plus gemcitabine versus gemcitabine for biliary tract cancer. N Engl J Med, 362(14): 1273-1281, 2010.
4) Morizane C , Okusaka T , Mizusawa J , et al.: Combination gemcitabine plus S-1 versus gemcitabine plus cisplatin for advanced/recurrent biliary tract cancer:the FUGA-BT (JCOG1113) randomized phase III clinical trial. Ann Oncol, 30(12): 1950-1958, 2019.
5) Sakai D , Kanai M , Kobayashi S , et al.: Randomized phase III study of gemcitabine, cisplatin plus S-1 (GCS) versus gemcitabine, cisplatin (GC) for advanced biliary tract cancer (KHBO1401-MITSUBA). Ann Oncol, 29:viii205–viii270, 2018.
6) エビデンスに基づいた 胆道癌診療ガイドライン.改訂第3版 ed,医学図書出版株式会社,東京,2019.
7) 高崎 健 , 小林 誠一郎 , 武藤 晴臣 ,他:拡大肝右葉切除兼膵頭十二指腸切除により切除し得た胆嚢癌5例の検討.胆と膵,1(7):923-932,1980.
8) Nimura Y , Hayakawa N , Kamiya J , et al.: Hepatopancreatoduodenectomy for advanced carcinoma of the biliary tract. Hepatogastroenterology, 38(2): 170-175, 1991.
9) Tsukada K , Yoshida K , Aono T , et al.: Major hepatectomy and pancreatoduodenectomy for advanced carcinoma of the biliary tract. Br J Surg, 81(1): 108-110, 1994.
10) Mizuno T , Ebata T , Yokoyama Y , et al.: Major hepatectomy with or without pancreatoduodenectomy for advanced gallbladder cancer. Br J Surg, 106(5): 626-635, 2019.
11) 水野 隆 , 尾上 俊 , 渡辺 伸 ,他:【胆嚢癌外科治療は進歩したか―現状と問題点―】肝膵十二指腸切除(HPD)の位置付け.胆と膵,41(9): 867-873,2020.
12) Shroff RT , Javle MM , Xiao L , et al.: Gemcitabine, Cisplatin, and nab-Paclitaxel for the Treatment of Advanced Biliary Tract Cancers:A Phase 2 Clinical Trial. JAMA Oncol, 5(6): 824-830, 2019.
13) Kato A, Shimizu H , Ohtsuka M , et al.: Surgical resection after downsizing chemotherapy for initially unresectable locally advanced biliary tract cancer: a retrospective single-center study. Ann Surg Oncol, 20(1): 318-324, 2013.
14) Kato A , Shimizu H , Ohtsuka M , et al.: Downsizing Chemotherapy for Initially Unresectable Locally Advanced Biliary Tract Cancer Patients Treated with Gemcitabine Plus Cisplatin Combination Therapy Followed by Radical Surgery. Ann Surg Oncol, 22 Suppl 3:S1093-S1099, 2015.
15) Varadhachary GR , Tamm EP , Abbruzzese JL , et al.: Borderline resectable pancreatic cancer:definitions, management, and role of preoperative therapy. Ann Surg Oncol, 13(8): 1035-1046, 2006.
16) Katz MH , Pisters PW , Evans DB , et al.: Borderline resectable pancreatic cancer:the importance of this emerging stage of disease. J Am Coll Surg, 206(5): 833-846 ; discussion 846-848, 2008.
PDFを閲覧するためには Adobe Reader が必要です。