日外会誌. 121(4): 435-441, 2020
特集
食道癌診療の現況と展望
6.胸部食道癌に対する低侵襲手術
|
東海大学医学部 消化器外科 小柳 和夫 , 小澤 壯治 , 二宮 大和 , 谷田部 健太郎 , 樋口 格 , 山本 美保 |
胸腔鏡や腹腔鏡を用いた食道癌内視鏡外科手術はMinimally Invasive Esophagectomy(MIE)と呼ばれ,本邦でも,その手術件数は増加傾向をたどっている.MIEに含まれる手術手技は多岐にわたり,胸腔鏡下,ロボット支援下,縦隔鏡下食道切除術などが代表的な手術術式として挙げられる.MIEでは,拡大視効果により,精細な手術が可能であり,根治性の向上につながることが期待される.また,体壁破壊の少なさは,術後合併症の軽減やQOLの維持に貢献すると考えられる.
MIEの短期成績,長期成績は,ともに良好な結果が示されている.胸腔鏡下手術では,開胸手術に比較し,手術時間は延長するものの,出血量は有意に減少することが示されている.術後肺合併症とsurgical site infectionの減少が認められ,QOLが維持され,長期的な予後も開胸手術と同等であった.ロボット支援下手術では,さらに多関節機能などにより,反回神経麻痺の軽減やリンパ節郭清精度の向上が期待される.縦隔鏡下手術は,手術時間が短く,片肺換気を必要としないことより,さらなる肺合併症の軽減が期待される.
MIEは,食道癌の根治とQOLの維持という,二つの大きな目標を達成可能な術式と考えられる.しかしながら,MIEは,高度な技能を必要とする手術手技であり,安全に手術を遂行するために,助手や手術室スタッフを含めたチームとしての手術技量の向上に取り組むことが重要である.
キーワード
胸部食道癌, 胸腔鏡下食道切除術, ロボット支援下手術, 縦隔鏡下手術
I.はじめに
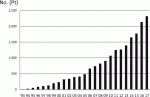
胸腔鏡や腹腔鏡を用いた食道癌内視鏡外科手術はMinimally Invasive Esophagectomy(MIE)として世界的に普及している1).日本内視鏡外科学会による内視鏡外科手術に関するアンケート調査(第13回集計結果報告)によれば,本邦でも食道癌に対する内視鏡外科手術件数は年々,増加傾向にある(図1)2).MIEでは体壁破壊が少ないため,患者に加わる手術侵襲が軽減でき,術後合併症の軽減やQOLの維持が期待される.
1992年にCuschieriらにより,最初のMIEの報告がなされたが3),その後,1990年代は安全性に関する検証が行われた.今世紀に入り,ハイボリューム施設から,開胸手術と遜色のない手術成績が報告されるようになり,2010年以降はクリニカルデータベースを用いた多数例の検討,Randomized Control Trial(RCT),そしてメタ解析を通して,MIEの有用性が示されつつある.MIEとして,胸腔鏡下手術が最も一般的に行われているが,近年では,ロボット支援下手術や縦隔鏡下手術も導入されてきており,臨床病期,患者の状態,施設方針に合わせて,それぞれの手術手技が選択されている.しかしながら,出血や他臓器損傷などの重篤な術中合併症も依然として一定の割合で認められており,安全で確実な手術操作を行えるように,日々の研鑽が必要である.
本稿では,胸部食道癌に対する低侵襲手術である胸腔鏡下,ロボット支援下,縦隔鏡下食道切除術の短期および長期成績を中心に,MIEの現状と今後の展望を解説する.
II.MIEの適応
胸腔鏡・腹腔鏡下食道切除術がMIEの代表的な術式であるが,その他にも小開胸を行うVideo-assisted Thoracoscopic Surgery(VATS)や,腹腔鏡による経裂孔的手術,縦隔鏡手術やロボット支援下手術なども含まれる.いずれの手技も,初期には術前無治療の早期症例を対象としていたが,技術と器具の進歩により,現在では進行癌にも適応を広げ,術前化学療法後や根治的化学放射線療法後の症例にも施行されるようになってきた.術中の他臓器損傷は開胸手術への移行を必要とするため,回避すべき事態であり,その点から,あきらかな他臓器浸潤癌や強度な肺癒着症例は適応から除外される.
III.胸腔鏡下食道切除術
胸腔鏡下食道切除術は,患者体位,術野の展開方法,内視鏡器具などを,施設毎にそれぞれ組み合わせて手術が行われている.体位として,大きく左側臥位と腹臥位があるが,近年は腹臥位を採用する施設が増加している.左側臥位の利点として,従来の開胸手術と同様の手術操作が可能であることが挙げられる.腹臥位では,重力と気胸効果による広い術野と外科医のエルゴノミクスが利点として挙げられる.一方で,腹臥位は緊急開胸へのコンバートが欠点に挙げられるが,われわれの施設では,半腹臥位からのベッドローテーションで腹臥位にすることにより,緊急開胸に対応している.
1.胸腔鏡下食道切除術の短期成績
胸腔鏡下食道切除術は拡大視効果が得られ,体壁破壊が少ないという特徴を有しており,開胸手術と比較した場合,出血量の減少や肺合併症軽減に有利と考えられる(表1).
本邦のNational Clinical Database(NCD)を用いた解析では,胸腔鏡下手術群は開胸手術群と比較して,手術時間が有意に長く,出血量が有意に少なかった4)5).また,術後48時間以上の人工呼吸器管理を要した症例とSurgical Site Infection(SSI)が胸腔鏡下手術群で有意に少なかった.Takeuchiらは術後無気肺が,Yoshidaらは総肺合併症が,それぞれ胸腔鏡下手術群で有意に少ないことを示した.いずれの報告も,手術手技に伴う合併症である縫合不全や反回神経麻痺に関して,胸腔鏡の有用性を示すことはできなかった.Yoshidaらの多数例の検討では,Takeuchiらの報告と異なり,30日以内の再手術割合に差は認めず,在院死亡は胸腔鏡下手術群で有意に少なかった.一方,オランダからのNational Databaseを用いた検討では,意外にも術後肺合併症には差を認めず,胸腔鏡下手術群で縫合不全と術後のreinterventionが有意に多かったと報告している6).Reinterventionが多かった理由として,約35%の症例がIvor-Lewis手術であったことが挙げられ,胸腔鏡下手術群で胃管壊死症例が多かったことが原因と推測された.また,郭清リンパ節個数は,胸腔鏡下手術群で有意に多かったと報告されている.
胸腔鏡下手術と開胸手術を比較したRCTであるTIME trialの結果では,やはり胸腔鏡下手術群は開胸手術群と比較して,手術時間が有意に長く,出血量が有意に少なかった7).また,術後2週間以内と在院中の肺感染症はともに胸腔鏡下手術群で有意に少なかった.手術手技に伴う合併症としては,縫合不全は差がなかったが,反回神経麻痺は胸腔鏡下手術群で有意な減少を認め,胸腔鏡による拡大視効果の有用性が示された.再手術や在院死亡に関しては差を認めず,郭清リンパ節個数も差を認めなかった.Nozakiらは,JCOG0502試験の副次解析を行い,総合併症発生割合は差を認めなかったが,無気肺は胸腔鏡下手術群が開胸群に比べて有意に少なかったと報告している8).また,再手術に関しては,反対に胸腔鏡下手術群で有意に多かった.
メタ解析による短期成績の検討でも,手術時間,出血量に関しては同様な結果であった9)10).また,術後合併症に関しては,総合併症発生割合,肺合併症発生割合,SSIが有意に胸腔鏡下手術群で少ないことが示されている.しかしながら,縫合不全,反回神経麻痺,乳び胸など,手術手技に伴う合併症に関しては差がなく,術後30日以内の死亡に関しても,有意な差は報告されていない.
これまでの報告では,胸腔鏡下食道切除術の短期成績の特徴は,術後肺合併症とSSIの減少と考えられる.これらはいずれも,体壁破壊の低減により得られる効果と示唆される.一方で,拡大視効果から,出血量の減少が得られていると示唆されるが,反回神経麻痺や乳び胸などの手術手技に伴う合併症軽減に関するエビデンスは少ない.また,再建臓器に関連した再手術の頻度も胸腔鏡下手術群で多いとの報告もなされており,手術手技の向上による改善が期待される.
2.胸腔鏡下食道切除術の長期成績
TIME trialの結果では,術後3年の無再発生存期間(Disease Free Survival:DFS),全生存期間(Overall Survival:OS)は,胸腔鏡下手術群と開胸手術群で差を認めなかった11)(表2).また,このTIME trialではQOLも検討しており,術後1年経過した時点で,胸腔鏡下手術群では,global QOLの改善が認められ,特に疼痛や会話において開胸手術群よりも有意に良好であった.このような結果は,胸腔鏡下食道切除術を食道癌手術に対して行うことを支持するものと結論している.Sunらは,胸腔鏡下食道切除術後患者を,翌日から経口摂取を開始する群と7日目から開始するRCTを行い,胸腔鏡下手術を受けた患者は,手術翌日から経口摂取が可能で,しかも手術翌日から経口摂取を開始した患者でglobal QOLの改善が認められたと報告している12).
胸腔鏡下手術と開胸手術を比較したメタ解析による長期成績の検討でも,DFS,OSともに両群で同等の結果であり,胸腔鏡下手術の手術精度は適切であると結論している10)13).
胸腔鏡下食道切除術は良好な長期成績が得られるとともに,術後合併症の軽減,QOLの維持が可能である.すなわち,食道癌の根治とともに,高い生活の質を担保することが可能な手術であると考えられ,食道癌の標準手術として施行している施設が多くなりつつある.本邦で行われているRCTの結果が待たれる14).


IV.ロボット支援下胸腔鏡下食道切除術
ロボット支援下胸腔鏡下食道切除術は,2018年度の保険収載以降,本邦においても手術症例が急激に増加している.ロボット支援下手術が有する多関節機能,手ぶれ防止機能,motion scaling等により,胸腔鏡下手術の動作制限などの欠点を補完することが期待される.しかしながら,ロボット支援下手術では触覚機能がないため,組織の把持,牽引には注意が必要である.欧米からは,すでに多くの報告がなされており,本邦でもさらに普及していくことが予想されるが,本邦のロボット支援下手術はいまだに黎明期であり,安全な手術手技が求められる.
ロボット支援下手術に関しても,胸腔鏡下手術と同様に,良好な短期成績が示されている(表3).ロボット支援下手術と開胸手術を比較したRCTの結果では,ロボット支援下手術群で,手術時間が有意に長く,出血量が有意に少なかった15).また,ロボット支援下手術群は,肺合併症,特に肺炎が有意に少なかった.しかしながら,手術手技に伴う合併症として,縫合不全,反回神経麻痺,乳び胸の発生割合に差を認めず,再手術や在院死亡に関しても両群間で差を認めなかった.退院後6週間目のQOLに関しては,ロボット支援下手術群で有意に良好であった.
ロボット支援下手術と胸腔鏡下手術を比較したメタ解析による短期成績の検討でも,術後合併症に有意な差は認めず,術後30日以内および在院死亡に関しても,有意な差は認められなかった16).しかしながら,ロボット支援下手術群において反回神経麻痺の発生割合が少なかったと報告されている.
また,ロボット支援下手術は縦隔リンパ節郭清に関して優れているとの報告が多い17)18).特に反回神経周囲リンパ節郭清におけるロボット支援下手術の有用性が示されている.
一方で,長期成績においては,開胸手術と同等のOSが示されており,現在,進行中の海外のRCTにおいても,おそらく胸腔鏡下手術の長期予後と同等の結果が期待される.
ロボット支援下胸腔鏡下食道切除術は,コンソール時間のラーニングカーブも短く,さまざまな機能により,従来の胸腔鏡下手術よりも,さらに精密な手術が可能と考えられ,反回神経麻痺の軽減,リンパ節郭清精度の向上につながると考えられる.

V.縦隔鏡下食道切除術
縦隔鏡下食道切除術では,胸腔鏡下手術と異なり,頸部創あるいは食道裂孔より体腔鏡を挿入し縦隔操作を行う.縦隔鏡下手術の利点は,従来,blunt dissectionと呼ばれた盲目的操作が,直視下操作になったことと,片肺換気を行う必要性がなく,肺合併症の軽減が期待されることが挙げられる.しかしながら,解剖学的に縦隔は狭く,食道の授動やリンパ節郭清を行うのに十分なスペースを得にくいという不利な面があったが,CO2ガスを用いた気縦隔法を用いることにより,広い術野と良好な視野を得ることができるようになった.
縦隔鏡下手術はリンパ節郭清,特に気管分岐部周囲で,胸腔鏡下手術より劣ると考えられてきたが,気縦隔法と手術器具の改良により,縦隔リンパ節郭清精度が向上した(表4).Fujiwaraら19),Moriら20)は,上縦隔リンパ節郭清個数の中央値は10個で,縦隔鏡下手術の反回神経周囲リンパ節郭清の妥当性を示した.体位変換がないことより,手術時間が短縮し,良好な術野で手術が行えることにより,出血量の軽減も認められた.そして,術後肺炎の発生も,期待したとおりに軽減することが示された.しかしながら,反回神経麻痺に関してはさまざまな報告があり,今後の検討が必要である.長期予後に関する検討は少ないが,Wangらは,中下部食道の深達度T2の腫瘍に対して検討し,縦隔鏡下手術と開胸手術のOSは同等であったと報告している21).
近年では,ロボット支援下による縦隔鏡下手術も導入され,縦隔鏡下食道切除術のさらなる発展が期待される.一方で,縦隔鏡下手術は縦隔操作に片肺換気を必要とせず,低侵襲外科治療としての重要なオプションであるが,手術適応や長期予後などに関する検討が必要である.

VI.おわりに
胸部食道癌に対する低侵襲治療として,胸腔鏡下,ロボット支援下,縦隔鏡下食道切除術の短期および長期成績を中心に述べた.MIEは,食道癌の根治とQOLの維持という,二つの大きな目標を達成可能な術式であり,今後も,さらに手術件数が増加するものと考えられる.しかしながら,MIEは,高度な技能を必要とする手術手技であり,安全に手術を遂行する必要がある.そのためには,手術適応,手術手順,周術期の管理に至るまで,しっかりとシミュレーションを行っておくことと,助手や手術室スタッフを含めたチームとしての手術技量の向上に取り組むことが重要である.
利益相反:なし
文献
1) Koyanagi K, Ozawa S, Tachimori Y: Minimally invasive esophagectomy performed with the patient in a prone position:a systematic review. Surg Today, 46: 275-284, 2016.
2) 日本内視鏡外科学会:内視鏡外科手術に関するアンケート調査―第13回集計結果報告―.日内視鏡外会誌,21: 689-711, 2016.
3) Cuschieri A, Shimi S, Banting S: Endoscopic oesophagectomy through a right thoracoscopic approach. J R Coll Surg Edinb, 37: 7-11, 1992.
4) Takeuchi H, Miyata H, Ozawa S, et al.: Comparison of short-term outcomes between open and minimally invasive esophagectomy for esophageal cancer using a Nationwide Database in Japan. Ann Surg Oncol, 24: 1821-1827, 2017.
5) Yoshida N, Yamamoto H, Baba H, et al.: Can minimally invasive esophagectomy replace open esophagectomy for esophageal cancer? Latest analysis of 24,233 esophagectomies from the Japanese National Clinical Database. Ann Surg, 2019. doi:10.1097/SLA.0000000000003222
6) Seesing MFJ, Gisbertz SS, Goense L, et al.: A propensity score matched analysis of open versus minimally invasive transthoracic esophagectomy in the Netherlands. Ann Surg, 266: 839-846, 2017.
7) Biere SS, van Berge Henegouwen MI, Maas KW, et al.: Minimally invasive versus open oesophagectomy for patients with oesophageal cancer:a multicentre, open-label, randomised controlled trial. Lancet, 379: 1887-1892, 2012.
8) Nozaki I, Mizusawa J, Kato K, et al.: Impact of laparoscopy on the prevention of pulmonary complications after thoracoscopic esophagectomy using data from JCOG0502:a prospective multicenter study. Surg Endosc, 32: 651-659, 2018.
9) Shanmugasundaram R, Hopkins R, Neeman T, et al.: Minimally invasive McKeown’s vs open oesophagectomy for cancer: A meta-analysis. Eur J Surg Oncol, 45: 941-949,2019.
10) Guo W, Ma X, Yang S: Combined thoracoscopic-laparoscopic esophagectomy versus open esophagectomy: a-meta-analysis of outcome. Surg Endosc, 30: 3873-3881, 2016.
11) Straatman J, van der Wielen N, Cuesta MA, et al.: Minimally invasive versus open esophageal resection: three-year follow-up of the previously reported randomized controlled trial: the TIME Trial. Ann Surg, 266: 232-236, 2017.
12) Sun HB, Li Y, Liu XB, et al.: Early oral feeding following McKeown minimally invasive oesophagectomy:An open-label, randomized, controlled, noninferiority trial. Ann Surg, 267: 435-442, 2018.
13) Patel K, Askari A, Moorthy K: Long-term oncological outcomes following completely minimally invasive esophagectomy versus open esophagectomy. Dis Esophagus, 2020. doi:10.1093/dote/doz113
14) Kataoka K, Takeuchi H, Mizusawa J, et al.: A randomized phase III trial of thoracoscopic versus open esophagectomy for thoracic esophageal cancer: Japan Clinical Oncology Group Study JCOG 1409. Jap J Clin Oncol, 46: 174-177, 2016.
15) van der Sluis PC, van der Horst S, May AM, et al.: Robot-assisted minimally invasive thoracolaparoscopic esophagectomy versus open transthoracic esophagectomy for resectable esophageal cancer:a randomized controlled trial. Ann Surg, 269: 621-630, 2019.
16) Jin D, Yao L, Yu J, et al.: Robotic-assisted minimally invasive esophagectomy versus the conventional minimally invasive one: A meta-analysis and systematic review. Int J Med Robot, 2019:e1988.
17) Suda K, Ishida Y, Kawamura Y, et al.: Robot-assisted thoracoscopic lymphadenectomy along the left recurrent laryngeal nerve for esophageal squamous cell carcinoma in the prone position:technical report and short-term outcomes. World J Surg, 36: 1608-1616, 2012.
18) Deng HY, Huang WX, Li G, et al.: Comparison of short-term outcomes between robot-assisted minimally invasive esophagectomy in treating middle thoracic esophageal cancer. Dis Esophagus, 31: 1-7, 2018.
19) Fujiwara H, Shiozaki A, Konishi H, et al.: Perioperative outcomes of single-port mediastinoscope-assisted transhiatal esophagectomy for thoracic esophageal cancer. Dis Esophagus, 30: 1-8, 2017.
20) Mori K, Aikou S, Yagi K, et al.: Technical details of video-assisted transcervical mediastinal dissection for esophageal cancer and its perioperative outcome. Ann Gastroenterol Surg, 1: 232-237, 2017.
21) Wang J, Wei N, Lu Y, et al.: Mediastinoscopy-assisted esophagectomy for T2 middle and lower thoracic esophageal squamous cell carcinoma patients. World J Surg Oncol, 16: 58, 2018.
PDFを閲覧するためには Adobe Reader が必要です。